Oppioidi per il dolore cronico non oncologico: raccomandazioni EFIC® di pratica clinica – Parte 1
Presentiamo in traduzione italiana la prima parte delle Raccomandazioni EFIC® sul ruolo degli oppioidi nella gestione del dolore cronico non oncologico (per la parte 2 clicca qui)
***
Winfried Häuser1,2 | Bart Morlion3 | Kevin E. Vowles4 | Kirsty Bannister5 | Eric Buchser6 | Roberto Casale7 | Jean-François Chenot8 | Gillian Chumbley9 | Asbjørn Mohr Drewes10 | Geert Dom11 | Liisa Jutila12 | Tony O‘Brien13 | Esther Pogatzki-Zahn14 | Martin Rakusa15 Thomas Tölle17 | Nevenka Krčevski Škvarč18
1Department Internal Medicine 1, Klinikum Saarbrücken, Saarbrücken, Germany
2Department of Psychosomatic Medicine and Psychotherapy, Technische Universität München, Munich, Germany
3Center for Algology & Pain Management, University Hospitals Leuven, Leuven, Belgium
4School of Psychology, Queen's University Belfast, Belfast, UK
5Institute of Psychiatry, Psychology and Neuroscience, King's College London, London, UK
6Pain Management and Neuromodulation Centre EHC Hospital, Morges, Switzerland
7Neurorehabilitation Unit, Department of Rehabilitation, HABILITA, Bergamo, Italy
8Department of General Practice, Institute for Community Medicine, University Medicine Greifswald, Germany
9Imperial College Healthcare NHS Trust, Charing Cross Hospital, London, UK
10Mech-Sense, Department of Gastroenterology & Hepatology, Aalborg University Hospital, Denmark
11Collaborative Antwerp Psychiatric Research Institute (CAPRI), Antwerp University, Antwerpen, Belgium
12Pain Alliance Europe, Finland
13College of Medicine & Health, University College Cork, Cork, Republic of Ireland
14Department of Anaesthesiology, Intensive Care and Pain Medicine, University Hospital Münster UKM, Munster, Germany
15Department of Neurology, University Medical Centre, Maribor, Slovenia
16Department of Physiotherapy, University of Sevilla, Sevilla, Spain
17Department of Neurology, Techhnische Universität München, München, Germany
18Department of Anesthesiology, Intensive Care and Pain Treatment, Faculty of Medicine of University Maribor, Maribor, Slovenia
Autore corrispondente:
Winfried Häuser, Internal Medicine 1, Klinikum Saarbrücken, D-66119 Saarbrücken, Germany.
Email: whaeuser@klinikum-saarbruecken.de
*Developed by European Pain Federation (EFIC). Endorsed by European Academy of Neurology (EAN), European Federation of Addiction Societies (EUFAS), European Federation of Psychologists’ Associations (EFPA), European Headache Federation (EHF), European Psychiatric Association (EPA), European Region - World Confederation of Physical Therapy (ER-WCPT), European Society of Anaesthesiology and Intensive Care (ESAIC), European Society of Physical and Rehabilitation Medicine (ESPRM), European Society of Regional Anaesthesia & Pain Therapy (ESRA) and Pain Alliance Europe (PAE).
………..
This is an open access article under the terms of the Creative Commons Attribution-NonCommercial-NoDerivs License, which permits use and distribution in any medium, provided the original work is properly cited, the use is non-commercial and no modifications or adaptations are made.
© 2021 The Authors. European Journal of Pain published by John Wiley & Sons Ltd on behalf of European Pain Federation - EFIC ®.
Eur J Pain. 2021;25:949–968.
Pubblicato online 2021 Mar 2. DOI: 10.1002/ejp.1736 - PMCID: PMC8248186- PMID: 33655607
***
Abstract
Background: L'uso di oppioidi per il dolore cronico non oncologico (CNCP) è complesso. In assenza di orientamenti paneuropei su questo tema, la European Pain Federation (EFIC) ha commissionato un position paper.
Metodi: Le raccomandazioni di pratica clinica sono state sviluppate da otto società scientifiche e da un'organizzazione di auto-aiuto dei pazienti sotto il coordinamento di EFIC. È stata effettuata una ricerca sistematica nella letteratura MEDLINE (fino a gennaio 2020). Vengono fornite due categorie di linee guida: raccomandazioni basate sull'evidenza (supportate da evidenze provenienti da revisioni sistematiche di studi randomizzati controllati o di studi osservazionali) e dichiarazioni di buona pratica clinica (GCP) (supportate da evidenze indirette o da serie di casi, studi caso-controllo ed esperienza clinica). Il sistema GRADE è stato applicato per passare dalle prove alle raccomandazioni. Le raccomandazioni e le dichiarazioni GCP sono state sviluppate da una task force multiprofessionale (tra cui infermieri, utenti dei servizi, medici, fisioterapisti e psicologi) e procedure formali in più fasi per raggiungere una serie di raccomandazioni di consenso. Le raccomandazioni di pratica clinica sono state esaminate da cinque revisori esterni provenienti dal Nord America e dall'Europa e sono state anche pubblicate per un commento pubblico.
Risultati: Le principali raccomandazioni di pratica clinica suggeriscono: (a) innanzitutto ottimizzare i trattamenti non farmacologici consolidati e gli analgesici non oppioidi e (b) considerare il trattamento con oppioidi se i trattamenti non farmacologici stabiliti o gli analgesici non oppioidi non sono efficaci e/o non tollerati e/o controindicati. Vengono presentate potenziali indicazioni e controindicazioni basate sull'evidenza e sul consenso clinico per il trattamento con oppioidi. Diciotto raccomandazioni GCP forniscono indicazioni per quanto riguarda la valutazione clinica, nonché la valutazione, il monitoraggio, la continuazione e l'interruzione del trattamento con oppioidi.
Conclusioni: Gli oppioidi rimangono un'opzione di trattamento per alcuni pazienti selezionati con CNCP sotto attenta sorveglianza.
Significato: Nel dolore cronico, gli oppioidi non sono né una cura universale né un'arma universalmente pericolosa. Dovrebbero essere utilizzati solo per alcune sindromi dolorose croniche non tumorali selezionate se le opzioni di trattamento non farmacologiche e farmacologiche stabilite hanno fallito nei pazienti con dolore supervisionato come parte di un approccio completo, multimodale e multidisciplinare al trattamento. Solo in questo contesto, la terapia con oppioidi può essere uno strumento utile per raggiungere e mantenere un livello ottimale di controllo del dolore in alcuni pazienti
1 | INTRODUZIONE
Nel 2017, la European Pain Federation (EFIC) ha pubblicato un position paper sull'uso appropriato di oppioidi nella gestione del dolore cronico (O'Brien et al., 2017). Il position paper non ha differenziato tra la gestione del cancro cronico e il dolore non oncologico (CNCP). L'importanza degli oppioidi nella gestione del dolore oncologico e nelle cure palliative è accettata a livello internazionale, sebbene la quantità e la qualità delle prove sull'uso di oppioidi per il trattamento del dolore oncologico siano molto deludenti (Wiffen et al., 2017).
La crisi degli oppioidi in Nord America (DeWeerdt, 2019) ha portato a un aggiornamento delle linee guida canadesi sugli oppioidi per CNCP (Busse et al., 2017; Furlan et al., 2010) e ad una linea guida dei Centers for Disease Control (CDC) degli Stati Uniti (Dowell et al., 2016), che si è concentrata sulla riduzione del danno in relazione alla prescrizione di oppioidi per CNCP. Inoltre, diversi autori statunitensi hanno discusso le loro preoccupazioni sul fatto che la crisi degli oppioidi rifletta le carenze dei sistemi sanitari nordamericani (Dasgupta et al., 2018; Sullivan & Howe, 2013).
Sebbene i Paesi europei siano lontani dalla crisi degli oppioidi in Nord America (Chenaf et al., 2019; Häuser et al., presentato; Kalkman et al., 2019; Record nazionali della Scozia, 2018; Rosner et al., 2019), ci sono crescenti preoccupazioni sulla sicurezza della terapia oppioide a lungo termine (LTOT) per i pazienti con CNCP (Ballantyne, 2016). Pertanto, l’EFIC ha incaricato una Task Force (TF) per aggiornare il proprio documento sull'uso appropriato di oppioidi specificamente per CNCP e per separarlo dal dolore da cancro. Nel 2019 sono stati pubblicati gli standard per la gestione del dolore correlato al cancro in tutta Europa dalla Task Force EFIC sul dolore da cancro (Bennett et al., 2019). Includendo altre società europee di professionisti sanitari, il documento è stato rinominato European Clinical Practice Recommendations (ECPRs).
Questo documento riguarda gli oppioidi per CNCP e mira a promuovere l'uso responsabile degli oppioidi per CNCP attraverso:
- discussione sul ruolo degli oppioidi nella gestione del CNCP.
- identificazione delle potenziali indicazioni, controindicazioni e consigli per l'interruzione degli oppioidi.
- raccomandazioni per la buona pratica clinica (GCP; ad es. dosaggio; selezione di oppioidi; monitoraggio degli effetti collaterali).
- discussione sul ruolo degli oppioidi in specifiche popolazioni di pazienti.
- raccomandazioni per la gestione di specifici eventi avversi da oppioidi.
1.1. Campo di applicazione
Lo scopo degli ECPR è quello di supportare un processo decisionale appropriato e, se giustificata, un'appropriata prescrizione di oppioidi per pazienti di qualsiasi età con dolore cronico (persistente o ricorrente >3 mesi) non oncologico. Il target di riferimento include:
- tutti gli operatori sanitari (medici, psicologi, infermieri, terapisti occupazionali, fisioterapisti, farmacisti) che supportano i pazienti con CNCP.
- coloro che assumono oppioidi (pazienti) e i loro cari.
- coloro che si interessano di politica di prescrizione degli oppioidi.
Queste raccomandazioni di pratica clinica discutono di tutti gli oppioidi orali e transdermici che possono essere prescritti per la gestione del dolore cronico in Europa (buprenorfina, codeina, fentanyl, idrocodone, idromorfone, metadone, morfina, ossicodone, polamidone, tilidina), compresi gli oppioidi con una modalità d'azione bidirezionale (tapentadolo e tramadolo). I prodotti di combinazione di oppioidi con altri analgesici, come il paracetamolo, non sono considerati. L'ECPR è focalizzato su LTOT per CNCP. Pertanto, non affronta la gestione del trattamento del dolore acuto o subacuto (<4 settimane) (compresi gli episodi di dolore acuto di malattie croniche come l'anemia falciforme), l'assistenza al fine vita o l'uso di oppioidi per condizioni non dolorose come il disturbo da uso di oppioidi.
Le definizioni di LTOT variano ampiamente. La maggior parte degli studi definisce a lungo termine l’uso di oppioidi per più di 12 settimane (Karmali et al., 2020). Sulla base della durata dello studio degli RCT, abbiamo fatto una classificazione per la durata della terapia con oppioidi per raccomandazioni basate sull'evidenza per la potenziale indicazione degli oppioidi: a breve termine (4-12 settimane), a medio termine (13-26 settimane), a lungo termine (>26 settimane).
1.2. Esclusione di responsabilità
Gli ECPR non hanno lo scopo di contraddire le linee guida basate sull'evidenza specifiche della malattia. Sono dichiarazioni di consenso di esperti piuttosto che una linea guida e incorporano l'esperienza dei membri della TF. I membri della TF riconoscono le conclusioni di solide linee guida basate sull'evidenza, ma le raccomandazioni di pratica clinica riconoscono che le risposte individuali alla terapia possono differire dalle risposte medie descritte nelle linee guida basate sull'evidenza. Gli ECPR rappresentano una dichiarazione di consenso degli operatori sanitari che lavorano con persone con dolore, forniscono una prospettiva esperta, riconoscendo le prove, per supportare il processo decisionale clinico.
Gli ECPR non rappresentano un regolamento di azione od omissione, che è stato concordato da un'istituzione giuridicamente legittima, fissato per iscritto e pubblicato. Non è vincolante per l'area giuridica di un'istituzione e non comporterà sanzioni definite, se non seguite. Le raccomandazioni diventano clinicamente efficaci solo se la forza della raccomandazione viene considerata e integrata nella cura individuale del paziente, incluso il processo decisionale condiviso con i pazienti. La decisione se una certa forza di raccomandazione debba essere seguita deve essere presa dai medici, considerando le circostanze dei singoli pazienti e le risorse disponibili.
2 | METODI
2.1. Composizione della task force
La TF comprendeva 17 membri (6 donne) provenienti da nove paesi europei (Nord, Centro, Europa orientale e meridionale e Regno Unito). Nove delegati sono stati nominati dal consiglio direttivo di EFIC. Il consiglio ha selezionato i delegati che sostengono e che sono critici con l'uso di oppioidi per CNCP. Sette delegati in rappresentanza dei membri dell'European Pain Forum (https://europeanpainfederation.eu/advocacy/current‐projects/european‐pain‐forum/) si sono offerti volontari per contribuire. Questi delegati sono stati selezionati in base alle loro competenze cliniche e/o scientifiche. Un delegato della Pain Alliance Europe (PAE) ha partecipato come rappresentante dei pazienti. La TF comprendeva la maggior parte delle professioni sanitarie (medicina, infermieristica, fisioterapia, psicologia) che si prendevano cura di pazienti con dolore cronico. Le specialità mediche dei medici erano anestesiologia, gastroenterologia, medicina generale / medicina di famiglia, medicina interna generale, neurologia, medicina del dolore, cure palliative, medicina fisica e riabilitativa, psichiatria, medicina psicosomatica (vedi tabella 1).
TABELLA 1 - Composizione della task force
|
Membro TF |
Genere |
Specialità |
Paese |
Nominato da |
Valutazione dei COI finanziari relativi all'argomento del documento |
|
Bannister, Kirsty |
Femmina |
Farmacologia |
Gran Bretagna |
EFIC |
Nessuno |
|
Buchser, Eric |
Maschio |
Anestesiologia |
Svizzera |
Società Europea di Anestesia Regionale |
Nessuno |
|
Casale, Roberto |
Maschio |
Medicina Fisica e Riabilitativa |
Italia |
Società Europea di Medicina Fisica e Riabilitativa |
Nessuno |
|
Chenot, Jean‐ François |
Maschio |
Medicina generale/Medicina di famiglia |
Germania |
EFIC |
Nessuno |
|
Chumbley, Gillian |
Femmina |
Allattamento |
Gran Bretagna |
EFIC |
Nessuno |
|
Destino, Geert |
Maschio |
Psichiatria |
Belgio |
Associazione europea di psichiatria E Federazione europea delle società di dipendenza |
Nessuno |
|
Drewes, Asbjorn |
Maschio |
Medicina Interna/Gastroenterologia |
Danimarca |
EFIC |
moderato |
|
Häuser, Winfried |
Maschio |
Medicina interna, Medicina psicosomatica |
Germania |
EFIC |
Nessuno |
|
Jutila, Liisa |
Femmina |
Rappresentante dei pazienti |
Finlandia |
Pain Alliance Europe |
Nessuno |
|
Krcevski‐Škvarč, Nevenka |
Femmina |
Medicina delle cure palliative |
Slovenia |
EFIC |
Nessuno |
|
Morlion, Bart |
Maschio |
Anestesiologia |
Belgio |
EFIC |
Moderato |
|
O'Brien, Tony |
Maschio |
Medicina delle cure palliative |
Irlanda |
EFIC |
Moderato |
|
Pogatzki-Zahn, Esther |
Femmina |
Anestesiologia |
Germania |
Società Europea di Anestesiologia |
Moderato |
|
Rakusa, Martin |
Maschio |
Neurologia |
Slovenia |
Accademia Europea di Neurologia |
Nessuno |
|
Suarez ‐Serrano, Carmen |
Femmina |
Fisioterapia |
Spagna |
Regione Europea della Confederazione Mondiale di Terapia Fisica |
Nessuno |
|
Tölle, Thomas |
Maschio |
Neurologia |
Germania |
EFIC |
Moderato |
|
Vowles, Kevin |
Maschio |
Psicologia |
Gran Bretagna |
Federazione europea delle associazioni di psicologi |
Nessuno |
Abbreviazione: EFIC, European Pain Federation.
2.2. Gestione dei conflitti di interesse
Tutti i membri della TF hanno dichiarato eventuali potenziali conflitti di interesse (COI) prima dell'inizio dell'aggiornamento utilizzando il modulo per la divulgazione di potenziali conflitti di interesse del Comitato internazionale degli editori di riviste mediche (http://www.icmje.org/conflicts di interesse/). I potenziali COI sono stati valutati in modo indipendente da due rappresentanti di EFIC (Sam Kynman, direttore esecutivo e il Prof. Hans Georg Kress, presidente del comitato etico), che non hanno partecipato allo sviluppo di questo documento. Le discrepanze sono state risolte consensualmente. Il grado di COI finanziari con le aziende farmaceutiche che producono oppioidi è stato classificato in nessuno, lieve, moderato, alto, definito come segue:
- Nessuna: nessuna interazione.
- Lieve: solo onorari per le conferenze.
- Moderato: comitato consultivo; supporto allo studio.
- Alta: brevetto; dipendente di un'azienda farmaceutica.
Dodici membri della TF non avevano COI, compresi i tre presidenti della TF (Häuser, Krcevski-Škvarč e Vowles). Cinque membri avevano COI finanziari moderati (Drewes, Morlion, O'Brien, Pogatzky-Zahn, Tölle).
Il supporto di segreteria per la stesura di questo position paper è venuto da EFIC. Il finanziamento di EFIC è dettagliato nelle sue relazioni annuali più recenti che possono essere trovate sul sito web EFIC https://europeanpainfederation.eu/how‐we‐work/annual‐report/. Il finanziamento del PAE è dettagliato in https://pae‐eu.eu/activities/.
2.3. Questioni chiave
Le questioni chiave da affrontare sono state definite da un ciclo Delphi della TF. Quattro recenti linee guida nazionali sugli oppioidi per CNCP(Canada, Francia, Germania, USA; Busse et al., 2017; Dowell et al., 2016; Moisset & Martinez, 2016; Häuser et al., 2020) sono state fornite ai membri della TF dal team di sintesi delle prove per informare il processo. Le questioni chiave sono delineate nel materiale supplementare 1.
2.4. Strategia di ricerca
Per la revisione di potenziali indicazioni e controindicazioni sugli oppioidi, ci siamo concentrati su revisioni sistematiche (con o senza meta-analisi) di studi randomizzati controllati (RCT) di oppioidi per CNCP con almeno 4 settimane di durata in doppio cieco e su studi di estensioni in aperto di questi studi con almeno 6 mesi di durata e su linee guida basate sull'evidenza relative alla gestione della CNCP. Il team di sintesi delle prove (Häuser, Welsch) ha condotto le ricerche. PubMed è stato cercato l'11 febbraio 2020 (dal 2015) con i termini di ricerca ['oppioide' E 'dolore cronico' E 'revisione sistematica']. PROSPERO è stato cercato l'8 marzo 2020 con i termini di ricerca ['oppioidi' e 'dolore cronico non oncologico'].
Per la sezione sulle situazioni speciali, abbiamo condotto una ricerca selettiva della letteratura in PubMed nell'aprile 2020 con il termine di ricerca ["oppioidi"] e il rispettivo termine della dichiarazione GCP.
La letteratura per gli ECPR è stata selezionata dai membri del team di sintesi delle prove. Gli elenchi di riferimento delle revisioni sistematiche e delle linee guida selezionate sono stati presi in considerazione anche per le raccomandazioni e le dichiarazioni di pratica clinica del documento di sintesi. Le discrepanze sono state risolte per consenso.
2.5. Sintesi delle prove
Il rappresentante dei pazienti è stato coinvolto nella definizione delle domande chiave, fornendo raccomandazioni e dichiarazioni di buona pratica clinica e nella valutazione della versione per il paziente delle raccomandazioni di pratica clinica.
Il team di sintesi delle prove ha creato riepiloghi delle prove basati sulle revisioni sistematiche selezionate. La selezione dei risultati di interesse si è basata sulle raccomandazioni del gruppo di scrittura ACTINPAIN dell'International Association for the Study of Pain's (IASP) Special Interest Group on Systematic Reviews in Pain Relief (Moore et al., 2010) e sulle linee guida sullo sviluppo clinico di medicinali destinati al trattamento del dolore dell'Agenzia europea per i medicinali (2017). Questi risultati includevano:
- Sollievo dal dolore dal basale del 30% o superiore
- L'impressione globale del paziente è molto migliorata o migliorata moltissimo
- Disabilità
- Tassi di abbandono per eventi avversi
- Eventi avversi gravi
- Morte
- Uso/dipendenza non medica.
Abbiamo utilizzato la revisione sistematica con la ricerca più recente di letteratura o il maggior numero di studi inclusi nelle analisi. Se riportato, il sistema GRADE è stato utilizzato per i riassunti delle prove per fornire una descrizione dei benefici e dei danni, insieme a una valutazione della certezza delle prove su base risultato per risultato (Langendam et al., 2013). Se non era disponibile alcuna valutazione GRADE, abbiamo utilizzato la valutazione UpToDate della qualità delle prove (UptoDate®, 2020a, 2020b).
2.5.1. Preferenze dei pazienti
Dal 22 maggio al 2 giugno 2020 Pain Alliance Europe (PAE) ha condotto un'indagine con alcuni Paesi membri (Spagna, Romania, Belgio, Regno Unito, Svezia e Finlandia) sull'importanza dei potenziali effetti positivi e negativi dell'assunzione di un nuovo farmaco per la gestione del dolore cronico. I potenziali effetti positivi e negativi dei farmaci (correlati agli oppioidi) sono stati selezionati da tre membri della TF (due medici, un rappresentante dei pazienti). In totale, hanno partecipato 131 membri PAE (78% donne). I dettagli dell'indagine sui pazienti sono delineati nel materiale supplementare 2. Gli effetti positivi e negativi importanti o molto importanti sono stati valutati come segue:
- Effetti positivi
- Sollievo dal dolore del 50% o più: 74% degli intervistati.
- Sollievo dal dolore del 30% o più: 92% degli intervistati.
- Miglioramento del funzionamento quotidiano: 91%.
- Miglioramento del sonno: 82%.
- Effetti negativi
- Sonnolenza: 66%.
- "Dipendenza": 58%.
- Problemi sessuali: 45%.
Inoltre, una ricerca in PubMed ['preferenze del paziente' E 'oppioidi' E 'CNCP') nel 6 febbraio 2020 ha prodotto 6 risultati. Abbiamo trovato una revisione sistematica, che ha classificato il sollievo dal dolore, la nausea e il vomito come esiti negativi altamente significativi negli studi. Quando considerato negli studi, l'effetto avverso dei cambiamenti di personalità è stato valutato come altrettanto importante. La stitichezza è stata valutata nella maggior parte degli studi ed è stato un risultato importante, ma secondario al sollievo dal dolore, nausea e vomito. Gli unici due studi che hanno valutato la dipendenza, l'hanno trovata meno importante per i pazienti rispetto al sollievo dal dolore (Goshua et al., 2018).
2.6. Sviluppo di raccomandazioni e dichiarazioni GCP
Questo documento include due categorie di linee guida: raccomandazioni basate sull'evidenza (supportate da evidenze provenienti da revisioni sistematiche di RCT o di studi osservazionali) e dichiarazioni GCP (supportate da evidenze indirette o da singoli RCT, serie di casi, studi caso-controllo o esperienza clinica). Abbiamo applicato il sistema GRADE per passare dalle prove alle raccomandazioni se fossero disponibili revisioni sistematiche con valutazioni GRADE (Andrews et al., 2013). Abbiamo utilizzato la valutazione UptoDate della qualità delle prove, se le revisioni sistematiche con valutazioni GRADE non erano disponibili (vedi Tabella 2). Tutti i membri della TF hanno completato l'esercitazione Uptodate® Grading (https://www.uptodate.com/home/grading‐tutorial#).
TABELLA 2 - Valutazione della qualità delle prove a sostegno secondo UptoDate®
|
Valutazione della qualità |
Razionale |
|
Forte |
Prove coerenti da studi randomizzati e controllati ben eseguiti o prove schiaccianti di qualche altra forma. È improbabile che ulteriori ricerche cambino la nostra fiducia nella stima dei benefici e dei rischi. |
|
Moderato |
Prove da studi randomizzati e controllati con limitazioni importanti (risultati incoerenti, difetti metodologici, indiretti o imprecisi) o prove molto forti di qualche altra forma. È probabile che ulteriori ricerche (se eseguite) abbiano un impatto sulla nostra fiducia nella stima dei benefici e dei rischi e possano modificare la stima. |
|
Basso |
Evidenze da studi osservazionali, esperienza clinica non sistematica o da studi randomizzati e controllati con gravi difetti. Qualsiasi stima dell'effetto è incerta. |
Nota
Le categorie generali che abbassano la qualità delle prove da RCT sono:
Problemi metodologici suscettibili di causare pregiudizi:
- Risultati incoerenti
- Indiretta delle prove
- Pochi eventi osservati
I fattori che possono aumentare la qualità delle evidenze dagli studi osservazionali sono:
- Grande entità dell'effetto
- Tutti i pregiudizi plausibili ridurrebbero un effetto dimostrato
- Gradiente dose-risposta
Raccomandazioni basate su dati concreti potrebbero essere formulate "a favore" o "contro". La forza di una raccomandazione potrebbe essere "forte" o "debole" (cfr. tabella 3). Per una forte raccomandazione, abbiamo notato: "Raccomandiamo". Per una raccomandazione debole, abbiamo notato: "Suggeriamo". Allo stesso modo, le dichiarazioni GCP potrebbero essere fatte "a favore" o "contro" con i termini "dovrebbe essere considerato" (valido per quasi tutti i pazienti) e "può essere considerato" (valido per la maggior parte dei pazienti) (vedi Tabella 3).
TABELLA 3 - Come utilizzare e comprendere le raccomandazioni e la dichiarazione di buona pratica clinica del position paper
|
Questo position paper fornisce ai medici prescrittori e ai pazienti una base per le decisioni sull'uso di oppioidi per gestire il dolore cronico non oncologico. I prescrittori, i pazienti e le altre parti interessate – in particolare le agenzie regolatorie o i tribunali – non dovrebbero considerare assolute le raccomandazioni e le dichiarazioni di buona pratica clinica contenute in questa linea guida. Nessuna linea guida può spiegare le caratteristiche uniche dei pazienti e le loro circostanze cliniche; Questa linea guida non intende sostituire il giudizio clinico. |
|
Una raccomandazione forte significa che i benefici superano chiaramente i rischi e gli oneri o viceversa. Indica che tutti o quasi tutti i pazienti pienamente informati sceglierebbero la linea d'azione raccomandata e indicano ai medici che la raccomandazione è appropriata per quasi tutti i pazienti. |
|
Una raccomandazione debole significa che benefici, rischi e oneri sono strettamente bilanciati o incerti. Indica che la maggior parte dei pazienti informati sceglierebbe la linea d'azione suggerita, ma una minoranza apprezzabile non lo farebbe. Con raccomandazioni deboli, i medici dovrebbero riconoscere che scelte diverse saranno appropriate per i singoli pazienti e dovrebbero aiutare i pazienti a prendere una decisione coerente con i loro valori e preferenze. |
|
Il termine "Dovrebbe essere considerato" in una dichiarazione di buona pratica clinica significa che la dichiarazione di buona pratica clinica è appropriata per quasi tutti i pazienti. |
|
Il termine "Può essere considerato" in una dichiarazione di buona pratica clinica significa che la dichiarazione di buona pratica clinica è appropriata per la maggior parte dei pazienti. |
La TF è consapevole dell'esistenza di controversie o disparità nell'interpretazione delle prove (ad esempio degli RCT per il CLBP). Pertanto, le nostre raccomandazioni basate sull'evidenza si basano anche sull'esperienza clinica.
2.7. Procedura di ricerca del consenso
Le raccomandazioni basate sull'evidenza e le dichiarazioni del GCP sono state inizialmente preparate dai tre presidenti della TF (Häuser, Krcevski-Skvarc e Vowles). Questi sono stati poi discussi, modificati e finalizzati dalla TF in sette round Delphi. I singoli membri della TF hanno poi votato online dal 1° al 12 giugno 2020. Il gruppo ha tenuto una conferenza finale di consenso basata sul web il 13 giugno 2020. Tutti i membri della TF hanno partecipato alla votazione online e tutti tranne uno alla conferenza di consenso basata sul web. In questa conferenza, tutte le dichiarazioni e le raccomandazioni che non hanno raggiunto un consenso del >90% nella votazione online sono state discusse e modificate se necessario con l'obiettivo di aumentare la forza del consenso. Per entrambe le procedure di voto, i membri della TF avevano tre opzioni: essere d’accordo, non essere d'accordo o astenersi (a causa della mancanza di esperienza). I voti di astensione non sono stati inclusi nei calcoli relativi alla forza del consenso.
La forza del consenso è stata classificata come segue: forte consenso: >95% di accordo; consenso: accordo 75%-95%; maggioranza: accordo 50%-75%; Nessun consenso: accordo ≤50%.
La forza del consenso è stata valutata in due modi: con e senza i voti dei membri con COI moderati. Nel documento, la forza del consenso per ogni raccomandazione e dichiarazione di pratica clinica è riportata come segue tra parentesi: (voti di tutti i membri della TF; voti di tutti i membri della TF senza COI).
2.8. Revisioni esterne
La bozza del documento ECPR è stata inviata a cinque persone con esperienza negli oppioidi per il dolore cronico, ognuna delle quali ha fornito una revisione aperta. Queste persone includevano Jane Ballantyne (USA), Andrea Furlan (Canada), Cathy Stannard (Regno Unito), Rainer Sabatowski (Germania) e Mark Sullivan (USA). A questi esperti è stato chiesto di identificare eventuali omissioni di argomenti importanti, commentare raccomandazioni basate su prove o GCP, fornire suggerimenti alternativi se necessario e commentare i metodi se importanti. I capi del TF hanno redatto le risposte ai revisori e suggerito modifiche alle raccomandazioni basate sull'evidenza, alle dichiarazioni GCP e ai commenti nel consenso. Tutte le proposte di modifica di questo documento sono state discusse dalla TF.
Sulla base dei commenti dei revisori, cinque dichiarazioni GCP (due sul ruolo degli oppioidi; una sugli oppioidi a breve durata d'azione; una sullo schema di assunzione; una sull’ iperalgesia indotta da oppioidi) sono state modificate per quanto riguarda il contenuto. È stata aggiunta una nuova dichiarazione GCP sul tapering degli oppioidi. È stato condotto un round Delphi della TF per valutare la forza del consenso di queste cinque dichiarazioni GCP modificate. La formulazione della forza della raccomandazione per le dichiarazioni GCP è stata modificata. La formulazione, ma non il contenuto, di undici dichiarazioni GCP è stata modificata. Sono stati inoltre ampliati ventisette commenti. Nelle sezioni "Contesto, campo di applicazione, clausola di esclusione della responsabilità" sono state apportate sei modifiche.
Sono stati ricevuti dodici commenti pubblici (11 da operatori sanitari, uno da un'azienda farmaceutica produttrice di un oppioide). Tutti i commentatori pubblici hanno dichiarato i loro conflitti di interesse finanziari (disponibili su richiesta): tutti i commenti sono stati esaminati e hanno ricevuto risposta dai presidenti della TF sulla base del consenso. Le risposte sono state discusse dai membri della TF. Diciassette commenti sono stati modificati (formulazione, supplementi) sulla base dei commenti degli operatori sanitari. Sulla base del commento della società farmaceutica, è stato apportato un supplemento nell'ambito di applicazione della sezione e sono stati modificati dieci commenti (formulazione, integratori). Abbiamo seguito uno dei sei suggerimenti dell'azienda, per menzionare il loro prodotto nel commento.
Le modifiche agli ECPR basate sui commenti dei revisori e dei commentatori pubblici possono essere fornite su richiesta.
2.9. Approvazione finale
Questi ECPR sono stati approvati dal consiglio direttivo di EFIC e dai consigli di nove società membri partecipanti del Pain Forum e della European Pain Alliance.
2.10. Pubblicazione e diffusione
Gli ECPR sono stati presentati all'European Journal of Pain in due parti. La prima parte copre il ruolo degli oppioidi nella gestione della CNCP, potenziali indicazioni e controindicazioni e GCP dell'uso di oppioidi. La seconda parte copre situazioni speciali, tra cui l'uso non medico e la dipendenza (Krcevski-Škvarc et al., 2021). Una versione breve per gli operatori sanitari sarà progettata dalla TF e sarà disponibile sulla pagina web di EFIC. Una versione del position paper per i non esperti sarà sviluppata con PAE.
3 | RISULTATI
3.1. Dichiarazioni e raccomandazioni di buona pratica clinica
3.1.1. Parte 1: Ruolo degli oppioidi nella gestione del dolore cronico non oncologico
- Ottimizzazione del trattamento non oppioide. Prima di prendere in considerazione il trattamento con oppioidi, suggeriamo innanzitutto di ottimizzare i trattamenti non farmacologici (ad es. esercizio fisico, fisioterapia, terapie psicologiche) e di considerare gli analgesici non oppioidi.Raccomandazione debole, forte consenso (16/16; 11/11).
Commento: L'ottimizzazione delle terapie non farmacologiche dovrebbe includere la terapia del dolore multimodale interdisciplinare (Kaiser et al., 2017) - se disponibile - e - in pazienti selezionati - procedure invasive come la neuromodulazione.
- Quando considerare gli oppioidi. Suggeriamo di prendere in considerazione una sperimentazione di oppioidi se i trattamenti non farmacologici consolidati e gli analgesici non oppioidi consolidati sono:
- Non efficace e/o
- Non tollerato e/o
- Controindicato
- Non disponibile
**Stabilito = Linea guida raccomandata o, se non disponibile, standard medico corrente.
Raccomandazione debole, forte consenso (15/15; 10/10).
Razionale: Non siamo a conoscenza di alcuna linea guida interdisciplinare basata sull'evidenza che raccomandi gli oppioidi come trattamento di prima linea per qualsiasi tipo di CNCP. Le terapie non farmacologiche, come l'esercizio fisico e le terapie psicologiche, sono state raccomandate come terapie di prima linea per le sindromi CNCP comuni come la lombalgia (Oliveira et al., 2018) o il dolore da osteoartrite (Gay et al., 2016). Sebbene gli approcci non farmacologici per il dolore cronico abbiano solo poco effetto con NNT che vanno da 4 a oltre 10 (Skelly et al., 2018), dovrebbero essere ottimizzati prima, dato che l'efficacia delle terapie farmacologiche per le sindromi CNCP come la lombalgia è limitata e associata a effetti collaterali potenzialmente significativi. Gli anticonvulsivanti sono stati raccomandati come terapia di prima linea per il dolore neuropatico (Finnerup et al., 2015). Devono essere considerati potenziali eventi avversi gravi come morte per overdose e dipendenza da oppioidi (Busse et al., 2012), sanguinamento gastrointestinale (Castellsague et al., 2012) ed eventi cardiovascolari da parte dei FANS (Bally et al., 2017), uso non medico di gabapentinoidi (Schjerning et al., 2016) e insufficienza epatica da antidepressivi (Darr & Sussman, 2020).
Riepilogo delle evidenze (per i dettagli vedere il materiale supplementare 3): PICO (Patient, Intervention, Comparator, Outcome): Qual è l'efficacia, la tollerabilità e la sicurezza degli oppioidi rispetto agli analgesici non oppioidi per CNCP in RCT della durata di almeno 4 settimane?
Una revisione sistematica degli RCT, confrontando oppioidi con analgesici non oppioidi, ha rilevato che gli analgesici non oppioidi erano superiori agli oppioidi in termini di miglioramento della funzione fisica e tollerabilità nella terapia a breve termine (4-12 settimane) del dolore neuropatico, lombare e osteoartrite (moderata qualità UptoDate) (Welsch et al., 2015). Questi risultati sono in linea con i risultati della recente revisione per conto dell'Agenzia statunitense per la ricerca e la qualità sanitaria (Chou et al., 2020).
- Selezione dei farmaci: La selezione dei farmaci dovrebbe considerare il tipo di CNCP, le comorbidità del paziente, le controindicazioni, le preferenze del paziente, i benefici e i danni delle terapie precedenti e il rapporto beneficio-rischio delle opzioni di trattamento farmacologico alternative disponibili.Dichiarazione di buona pratica clinica. Forte consenso (16/16; 11/11)
Commento: C'è una marcata variazione inter-individuale nella risposta/tollerabilità di tutti gli analgesici, compresi vari oppioidi, che non è prevedibile prospetticamente. Una serie di fattori può influenzare la scelta dell'oppioide da parte del medico all'inizio del trattamento, tra cui:
- Preferenza del clinico, spesso basata su familiarità, disponibilità e costi
- Via di consegna richiesta – ad esempio orale (preferito), ma in alcuni casi può essere selezionata una somministrazione transdermica per facilitare la somministrazione e ridurre il carico di farmaci orali, ecc.
- Comorbidità del paziente (vedere paragrafo sulle situazioni particolari)
- Potenziali indicazioni
Osservazioni preliminari:
- Tutte le potenziali indicazioni citate di seguito dovrebbero essere considerate solo alla luce delle raccomandazioni sul ruolo degli oppioidi nella gestione della CNCP.
- CNCP è un termine descrittivo che copre molte condizioni mediche dolorose che variano nella presentazione clinica e nei meccanismi fisiopatologici sottostanti, inclusa l'assenza di meccanismi sottostanti identificabili. La task force congiunta IASP-OMS che ha sviluppato i nuovi concetti del sistema di classificazione del dolore cronico ha suggerito una distinzione tra dolore cronico primario (malattia a sé stante) e dolore cronico secondario (dolore come sintomo di una malattia di base). Il principale meccanismo fisiopatologico delle sindromi dolorose primarie è il dolore nociplastico e delle sindromi dolorose croniche secondarie nocicettive e/o neuropatiche (Nicholas et al., 2019; Treede et al.,2019; Trouvin & Perrot, 2019). Il dolore nociplastico è definito da dolore che (1) deriva da nocicezione alterata nonostante nessuna (2) chiara evidenza di danno tissutale effettivo o minacciato che causa l'attivazione di nocicettori periferici o (3) evidenza di malattia o lesione del sistema somatosensoriale che causa il dolore (Kosek et al., 2016).
La distinzione tra dolore primario e secondario può essere una semplificazione eccessiva. In alcuni pazienti con dolore secondario cronico, come l'osteoartrite o il dolore post-infortunio, i meccanismi nociplastici svolgono un ruolo (Moore et al., 2020; Woolf, 1983). L'input nocicettivo in corso, ad esempio, da infiammazione articolare di basso grado, può svolgere un ruolo nella cosiddetta fibromialgia secondaria (comorbidità) (Fitzcharles et al., 2018) che è considerata un prototipo di una sindrome da dolore nociplastico (Nicholas et al., 2019).
A causa della diversità delle sindromi CNCP, il position paper aggiornato segue l'approccio delle linee guida francesi e tedesche (Häuser et al., 2020; Moisset & Martinez, 2016), per suddividere il CNCP in diverse entità cliniche per quanto riguarda le potenziali indicazioni e controindicazioni degli oppioidi.
4.1 Suggeriamo di prendere in considerazione gli oppioidi per le sindromi dolorose croniche secondarie elencate di seguito. Raccomandazione debole
Riepilogo delle prove (per i dettagli si veda il materiale supplementare 4):
PICO: Qual è l'efficacia, la tollerabilità e la sicurezza degli oppioidi rispetto al placebo in pazienti di qualsiasi età con CNCP?
Ci sono prove GRADE di qualità da bassa a molto bassa da 21 RCT di 4-15 settimane con 7.650 partecipanti che gli oppioidi sono superiori nel ridurre il dolore e la disabilità, inferiori nella tollerabilità e non diversi in sicurezza rispetto al placebo per il dolore CLBP (Petzke et al., 2020) (Materiali supplementari 1 e 2).
Ci sono prove di GRADE di qualità da bassa a molto bassa da 22 RCT di 4-26 settimane con 8.942 partecipanti che gli oppioidi sono superiori nel ridurre il dolore e la disabilità, inferiori nella tollerabilità e non diversi in sicurezza rispetto al placebo per il dolore OA (Welsch et al., 2020).
Ci sono prove di GRADE di qualità da bassa a molto bassa da 16 RCT di 4-12 settimane con 2.199 partecipanti che gli oppioidi sono superiori nel ridurre il dolore e la disabilità, inferiori nella tollerabilità e non diversi in sicurezza rispetto al placebo per alcune sindromi dolorose neuropatiche (Sommer et al., 2020).
Ci sono prove GRADE di qualità molto bassa da 15 studi di estensione in aperto della durata fino a 4 anni con 3.590 partecipanti che in pazienti auto-selezionati con lombalgia cronica, dolore neuropatico e OA, le riduzioni del dolore e della disabilità possono essere mantenute. Il tasso di abbandono a causa di eventi avversi e decessi aumenta con la durata dello studio (Bialas et al., 2020).
Il basso tasso di eventi avversi gravi negli RCT con oppioidi è in netto contrasto con i risultati di studi osservazionali in Nord America che hanno dimostrato importanti rischi di sovradosaggio non fatale e fatale non intenzionale, dipendenza fisica molto frequente e dipendenza frequente (Busse et al., 2017). I dati di assistenza clinica di routine di alcuni Paesi europei non hanno mostrato segnali di un'epidemia di oppioidi (Bedene et al., 2019; Chenaf et al., 2019; Kalkman et al., 2019; Rosner et al., 2019).
Le possibili spiegazioni di queste divergenze sono le seguenti:
- La maggior parte degli RCT ha escluso i pazienti con abuso di sostanze attuale o con una storia di abuso di sostanze e con gravi malattie mediche. Queste (relative) controindicazioni per gli oppioidi potrebbero essere state trascurate nelle cure mediche di routine in Nord America. Gli oppioidi sono stati prescritti alla parte più vulnerabile della popolazione (disoccupazione, povertà, problemi di salute mentale) (deWeerdt,2019).
- La sorveglianza dei pazienti nel contesto degli studi clinici è più stretta di quella nell'assistenza clinica di routine.
- Esistono differenze nei sistemi sanitari tra il Nord America e l'Europa (ad esempio, disponibilità di trattamenti non farmacologici; aspettative dei pazienti di ottenere la prescrizione di farmaci; benefici finanziari aumentando il numero di pazienti con prescrizioni di oppioidi).
- La maggior parte degli RCT non ha valutato sistematicamente l'uso non medico e la dipendenza o il disturbo da uso di oppioidi e pertanto potrebbe aver sottovalutato la loro prevalenza.
|
Entità clinica (codice ICD-10) |
Qualità delle evidenze (GRADE) |
Forza del consenso |
|
Mal di schiena cronico con meccanismi di dolore nocicettivo e/o neuropatico predominante un (M42.16‐M41.19, M42.90, M42.96‐99, M43.0, M43.1, M47.26, M47.27, M47.29, M47.86, M47.87, 47.88, M47.99, M48.06, M48.2, M54.16, M54.5, M55.3, M.99.33; M99.43, M99.53) |
Basso |
Consenso (16/17; 11/15) |
|
Dolore cronico da osteoartrite (M15-19) |
Da molto bassa a bassa |
Consenso (13/14; 8/9) |
|
Polineuropatia diabetica dolorosa cronica (G 63.2) |
Molto basso |
Consenso/Maggioranza (11/14; 6/9) |
|
Nevralgia posterpetica (B02.2) |
Molto basso |
Consenso/Maggioranza (11/14; 6/9) |
La lombalgia cronica aspecifica con meccanismi di dolore nociplastico predominante è molto più frequente della lombalgia cronica specifica con meccanismi di dolore nocicettivo e / o neuropatico predominanti (Maher et al., 2017). Come indicato nella sezione "Potenziali controindicazioni", gli oppioidi non sono indicati per la lombalgia aspecifica
4.2. Gli oppioidi possono essere considerati per le sindromi dolorose croniche secondarie elencate di seguito. Dichiarazioni di buona pratica clinica
Nota preliminare: è necessaria un'analisi del rischio e del beneficio prima di intraprendere la terapia con oppioidi per le diagnosi elencate di seguito.
|
Entità clinica (codice ICD-10) |
Qualità delle prove (UptoDate) |
Dichiarazione di pratica clinica |
Forza del consenso |
|
Dolore cronico dopo lesione del midollo spinale (S24)a |
Moderato b |
Può essere considerato |
Consenso (11/13; 6/8) |
|
Polineuropatia cronica non diabetica (G60-64)a |
Moderato c |
Può essere considerato |
Consenso (11/12; 6/7) |
|
Dolore cronico all'arto fantasma (G54.6) a |
Moderato b |
Può essere considerato |
Consenso/Maggioranza (10/12; 5/7) |
|
Dolore radicolare cronico (M54.1) a |
Moderato c |
Può essere considerato |
Consenso (11/12; 6/7) |
|
Dolore cronico nell'artrite reumatoide (M06.‐) a |
Moderato b |
Può essere considerato |
Consenso (13/13; 8/8) |
|
Dolore cronico nella malattia di Parkinson (G20, 21) a |
Moderato b |
Può essere considerato |
Consenso (12/13; 7/8) |
|
Dolore cronico nella sindrome delle gambe senza riposo (G25) a |
Moderato b |
Può essere considerato |
Consenso (11/12; 6/7) |
|
Dolore cronico dovuto a lesioni cerebrali (ad es. stato post ictus talamico, sclerosi multipla) |
Basso d |
Può essere considerato |
Consenso (10/11; 5/6) |
|
Dolore cronico da sindrome dolorosa regionale complessa (CRPS), tipi I e II (G90.5, G90.6) |
Basso d |
Può essere considerato |
Consenso (12/13; 7/8 |
|
Cefalea secondaria cronica (ad es. dopo emorragia subaracnoidea) (G44.8) |
Basso d |
Può essere considerato |
Consenso (10/11; 5/6) |
|
Dolore cronico da osteoporosi (ad es. nuove fratture del corpo vertebrale) (M80.‐) |
Basso d |
Può essere considerato |
Forte consenso (13/13; 8/8) |
|
Dolore cronico dovuto ad altre malattie reumatiche infiammatorie ad eccezione dell'artrite reumatoide (ad es. lupus eritematosi sistemica, spondiloartrite sieronegativa) (M45-M49) |
Basso d |
Può essere considerato |
Forte consenso (12/12; 7/7) |
|
Dolore post-chirurgico cronico (ad es. sindrome post-toracotomia, post-sternotomia e postmastectomia, e dopo chirurgia addominale, facciale o ernia) (T80-88) |
Basso d |
Può essere considerato |
Consenso (11/13; 6/8) |
|
Dolore cronico da malattia occlusiva arteriosa ischemica o infiammatoria (I70-I79) |
Basso d |
Può essere considerato |
Forte consenso (11/11;6/6) |
|
Dolore cronico da ulcere da decubito di grado 3 e 4 (L 89) |
Basso d |
Può essere considerato |
Forte consenso (13/13; 8/8) |
|
Dolore cronico da contratture fisse in pazienti infermieristici dipendenti (M67) |
Basso d |
Può essere considerato |
Consenso (10/11; 5/6) |
|
Neuropatia cronica post-traumatica del trigemino (G 50.9) |
Basso d |
Può essere considerato |
Consenso (11/13; 6/8) |
|
Dolore pelvico cronico da aderenze estese (N73.6) e/o endometriosi estesa e/o infiltrante (N80.x) |
Basso d |
Può essere considerato |
Consenso/Maggioranza (10/12; 5/7) |
a Cfr. materiale supplementare 5.
b Un RCT disponibile.
c Due RCT disponibili.
d Nessun RCT disponibile; Consenso degli esperti.
Razionale: Gli oppioidi ottengono miglioramenti del dolore e della funzione rispetto al placebo al costo di una minore tollerabilità nella lombalgia cronica e nel dolore da osteoartrite e in alcune sindromi dolorose neuropatiche. Nel contesto degli RCT e della stretta sorveglianza clinica, gli oppioidi possono essere considerati ragionevolmente sicuri.
Per tutte le altre condizioni mediche con meccanismi di dolore nocicettivo e/o neuropatico, le prove per l'uso di oppioidi si basano su singoli RCT per alcune sindromi dolorose neuropatiche e sull'esperienza clinica per tutte le altre condizioni mediche.
Sintesi delle prove (cfr. materiale supplementare 5):
- Potenziali controindicazioni: gli oppioidi non devono essere considerati per le sindromi dolorose primarie.Dichiarazione di buona pratica clinica
Razionale: Per sindromi dolorose primarie: (a) La nostra ricerca sistematica ha trovato solo un RCT ciascuno con tramadolo (Russell et al., 2000) e tramadolo / paracetamolo (Bennett et al., 2003) per una sindrome da dolore nociplastico (FMS). Il tramadolo ha un'ulteriore modalità d'azione (inibitore della ricaptazione della serotonina e della noradrenalina) che potrebbe spiegare l'efficacia trovata (Walitt et al., 2016). (b) Studi di coorte hanno dimostrato che l'uso di oppioidi è associato a un esito clinico negativo nell'emicrania (Ashina, 2019; Minen et al., 2014) e fibromialgia (Fitzcharles et al., 2013). (c) Le linee guida scoraggiano l'uso di oppioidi, ad esempio per IBS (Drossman, 2019), fibromialgia (MacFarlane et al., 2017) o emicrania (American Headache Society, 2019). (d) I pazienti con sindromi dolorose primarie possono essere meno sensibili agli oppioidi a causa di livelli endogeni più elevati di oppioidi e più suscettibili al peggioramento dell'iperalgesia da oppioidi (Toubia & Khalife, 2019).
|
Condizioni mediche (codice ICD-10) |
Qualità delle prove (UptoDate) |
Dichiarazione di pratica clinica |
Forza del consenso |
|
Cefalea primaria (emicrania, cefalea tensiva) (G43.x, G44.0, G44.2, G44.8) |
Basso |
Non dovrebbe essere considerato |
Consenso/Forte consenso (15/16; 11/11) |
|
Altra cefalea primaria cronica o dolore orofacciale (disturbo dell'articolazione temporo-mandibolare, dolore orofacciale cronico primario [dolore facciale atipico]) (M26.60, G50.1) |
Basso |
Non dovrebbe essere considerato |
Forte consenso (14/14; 9/9) |
|
Disturbi somatici funzionali (ad es. sindrome fibromialgica, sindrome dell'intestino irritabile) (M79.70; F45.32/K58.0/K58.1) |
Basso |
Non dovrebbe essere considerato |
Consenso/forte consenso (14/15; 9/9) |
|
Altre sindromi da dolore viscerale cronico primario (dolore toracico cronico primario [dolore toracico atipico], sindrome da dolore epigastrico primario cronico [dispepsia funzionale], sindrome da dolore cronico primario alla vescica [vescica iperattiva], sindrome da dolore pelvico cronico primario [dolore pelvico e perineale] (R07.89. K30, N32.81, R102.] |
Basso |
Non dovrebbe essere considerato |
Forte consenso (14/14; 9/9) |
|
Sindromi dolorose muscoloscheletriche croniche primarie (cervicale, toracico, lombalgia, dolore agli arti) (non sono disponibili codici ICD-10 corrispondenti) |
Basso |
Non dovrebbe essere considerato |
Consenso/forte consenso (14/15; 9/9) |
|
Dolore cronico come manifestazione principale di un disturbo mentale (depressione atipica, disturbo del dolore somatoforme persistente, disturbo d'ansia generalizzato, disturbo da stress post-traumatico) (F41, F43, F32, F33, F45) |
Basso |
Non dovrebbe essere considerato |
Forte consenso (15/15; 10/10) |
- Questioni controverse
La TF non è riuscita a raggiungere un consenso sulle potenziali indicazioni o controindicazioni degli oppioidi per la gestione del dolore nella pancreatite cronica e nella malattia infiammatoria cronica intestinale (principalmente il morbo di Crohn). C'è stato un consenso sul fatto che gli oppioidi dovrebbero essere utilizzati in pazienti selezionati solo dopo una valutazione specialistica interdisciplinare come parte di un approccio terapeutico multimodale e con stretta sorveglianza.
Pancreatite cronica: in un RCT che confronta morfina e fentanyl, entrambi i farmaci non hanno ridotto significativamente il dolore e la disabilità (Niemann et al., 2000). Negli studi di coorte statunitensi, l'uso di oppioidi è stato associato al disturbo da uso di oppioidi (Bilal et al., 2019). Secondo l'esperienza clinica, fino al 25% dei pazienti può sperimentare sollievo dal dolore associato all'uso di oppioidi (Drewes et al., 2017). Pertanto, gli oppioidi possono essere utilizzati in pazienti selezionati sotto stretta sorveglianza per un tempo limitato seguendo le stesse raccomandazioni utilizzate per altre sindromi dolorose. Poiché molti pazienti hanno dolore postprandiale o peggioramento intermittente del dolore di fondo, il trattamento con oppioidi a rilascio immediato per periodi più brevi è probabilmente migliore degli oppioidi a rilascio controllato che possono comportare un rischio più elevato di dipendenza. Tuttavia, circa il 50% dei pazienti ha una storia di disturbo da uso di alcol (Olesen et al., 2019) e circa il 20% continua ad avere un consumo eccessivo di alcol (Olesen et al., 2020). Questo sottogruppo di pazienti può avere un elevato potenziale di disturbi da uso di sostanze e gli oppioidi – se prescritti – devono essere utilizzati con un elevato livello di controllo e attenzione.
Malattie infiammatorie intestinali: il dolore di lunga durata è raramente un problema nei pazienti con colite ulcerosa a meno che non si verifichino gravi complicanze, ma i pazienti con malattia di Crohn possono soffrire di forti dolori cronici dovuti a infiammazione, stenosi e stenosi dell'intestino. In uno studio di coorte statunitense, i pazienti hanno riportato la stessa intensità di dolore addominale con e senza oppioidi (Coates et al., 2020), ma questo può riflettere confusione per indicazione in quanto gli oppioidi sono probabilmente somministrati a pazienti con più dolore e lo studio ha avuto un disegno retrospettivo. In uno studio di coorte retrospettivo britannico, la mortalità è aumentata in caso di dosaggio elevato o moderato di morfina rispetto ai controlli abbinati alla propensione (Burr et al., 2018). I problemi con il dolore viscerale e gli oppioidi sono principalmente legati ai loro effetti collaterali sull'intestino e ai problemi di motilità, trasporto di liquidi e funzione sfinterica (Farmer et al., 2019). Questo è spesso un grosso problema nei pazienti con malattia di Crohn in cui stenosi e stenosi dell'intestino possono peggiorare gli effetti collaterali indotti dagli oppioidi. Per riassumere, gli oppioidi possono essere considerati per il trattamento a breve termine del dolore in caso di riacutizzazioni acute in pazienti con malattia di Crohn, ma l'uso di oppioidi a lungo termine può essere associato a scarsi risultati. La linea guida della British Society of Gastroenterology scoraggia l'uso di oppioidi per la gestione del dolore nelle malattie infiammatorie intestinali (Lamb et al., 2019).
3.1.2. Parte 2: Buona pratica clinica
- Misure preliminari all'inizio dell'assunzione di oppioidi
1.1 Anamnesi e stato clinico: devono essere considerati e documentati i casi generali (incluso il precedente disturbo da uso di sostanze), l'anamnesi correlata al dolore e lo stato fisico e psicologico del paziente. Dichiarazione di buona pratica clinica. Forte consenso (17/17; 17/17).
Strumento di pratica (facoltativo): Breve inventario del dolore Versione breve: http://www.npcrc.org/files/news/briefpain_short.pdf
1.2 Screening per disturbi mentali: Il medico che sta pensando alla prescrizione di oppioidi dovrebbe prendere in considerazione la documentazione della storia psicosociale e lo screening per i disturbi psichiatrici attuali e / o passati. Dichiarazione di buona pratica clinica. Forte consenso (17/17; 17/17).
Strumento pratico (facoltativo): questionario sulla salute del paziente 4. https://www.oregonpainguidance.org/app/content/uploads/2016/05/PHQ‐4.pdf
1.3 Esame di salute mentale: nel caso di indicazioni di un disturbo mentale (disturbi depressivi e d'ansia, disturbo da uso di sostanze) dovrebbe essere considerato di offrire al paziente una consulenza con uno specialista di salute mentale a seconda delle risorse locali e della tradizione. Dichiarazione di buona pratica clinica. Forte consenso (17/17; 17/17).
Razionale: I disturbi di salute mentale aumentano il rischio di abuso di oppioidi prescritti (Cragg et al., 2019).
1.4 Obiettivi terapeutici. I medici che prescrivono oppioidi dovrebbero prendere in considerazione la definizione di obiettivi terapeutici individuali e realistici insieme al paziente. Dichiarazione di buona pratica clinica. Forte consenso (17/17; 17/17).
Razionale: La definizione degli obiettivi terapeutici include la considerazione del sistema di convinzione dei pazienti per quanto riguarda l'efficacia degli oppioidi. I pazienti con CNCP possono avere aspettative non realistiche per il sollievo dal dolore basato sui farmaci, ad esempio il sollievo completo dal dolore. Da un punto di vista medico, obiettivi terapeutici ragionevoli (= risposta terapeutica) sono miglioramenti individualmente significativi nella funzione quotidiana (ad es. ritorno al lavoro, "essere in grado di falciare di nuovo il prato", "essere in grado di prendersi cura di se stessi di nuovo"). Gli obiettivi possono anche includere sollievo dal dolore del 30% o superiore, sebbene la riduzione del dolore come obiettivo terapeutico sia stata oggetto di alcuni dibattiti (Ballantyne & Sullivan, 2015).
1.5 Informazioni per i pazienti: i medici che prescrivono oppioidi dovrebbero prendere in considerazione la possibilità di fornire ai pazienti informazioni mediante comunicazioni orali o scritte documentate, comprese informazioni sugli aspetti relativi al traffico e al luogo di lavoro rilevanti per il paziente (e potenzialmente per la famiglia e / o il caregiver). Dichiarazione di buona pratica clinica. Forte consenso (17/17; 17/17).
Commento: È probabile che le informazioni funzionino meglio se sono facilmente comprensibili dai pazienti e brevi.
Le informazioni per i pazienti possono includere:
- Istruzioni relative ai tempi esatti e al dosaggio del farmaco; durata dell'azione del farmaco; istruzioni da seguire in caso di dimenticanza della dose
- Indicazioni di interazioni con altri farmaci tra cui over-the-counter farmaci e sostanze illecite
- Trattamento profilattico delle reazioni avverse ai farmaci, come la stitichezza
- Cessazione del consumo di alcol o sedativo senza previa discussione con il medico
- Responsabilità del paziente, come una buona aderenza al piano di trattamento, feedback regolare al medico curante; per esempio, sotto forma di un diario del dolore
- Conservazione sicura degli oppioidi
- Istruzioni su come smaltire in modo sicuro gli oppioidi non utilizzati dal paziente in conformità con le pertinenti normative legali sugli stupefacenti
- Aspetto legale relativo alla distribuzione di farmaci contenenti oppioidi
- Assunzione di farmaci contenenti oppioidi all'estero
- Possibile influenza negativa sulla capacità di guidare, nonché sulle attività sul posto di lavoro (per es. lavoro con le macchine, attività di controllo) e durante il tempo libero (per es. lavori domestici, giardinaggio, sport)
- Potenziali danni a breve e lungo termine
Commento: I pazienti devono essere informati che guidare sotto dosi stabili di oppioidi non può essere compromesso in generale e che il paziente ha la responsabilità di controllare se stesso a priori, se si sente idoneo a guidare o meno. Devono inoltre essere fornite informazioni sull'impatto della menomazione dovuta ad altre condizioni di salute (come malattie mentali, compromissione della funzione motoria) e co-medicazione (come benzodiazepine, farmaci antidepressivi). La meta-analisi degli studi sperimentali ha dimostrato che ci sono molti fattori che influenzano il grado di compromissione causata dal consumo di farmaci (ad esempio agente attivo, galenica, via di somministrazione, dose, tempo di somministrazione, periodo di tempo tra la somministrazione e il requisito di prestazione, conformità e disposizione del paziente, nonché uso concomitante di farmaci aggiuntivi) (Ramaekers et al., 2006).
1.6 Titolazione e sicurezza di guida: i medici che prescrivono oppioidi dovrebbero prendere in considerazione la possibilità di informare il paziente delle normative legali nazionali relative alla guida durante la fase di titolazione o quando la dose viene modificata e di documentare le informazioni nella tabella. Dichiarazione di buona pratica clinica. Forte consenso (17/17; 17/17).
Commento: La fase di titolazione/inizio degli oppioidi, inclusa la variazione della dose (verso l'alto, verso il basso) o il passaggio da oppioidi sono le fasi più vulnerabili del deterioramento funzionale/cognitivo dovuto al trattamento con oppioidi (Bruera et al., 1989; Ramaekers et al., 2006).
- Trattamento con oppioidi
2.1 Numero di medici prescrittori: I medici che prescrivono gli oppioidi possono prendere in considerazione la prescrizione di oppioidi da parte di un solo medico alla volta, quando possibile, o da parte di un medico dello stesso team clinico o di un sostituto se il prescrittore designato è in congedo. Forte consenso (16/16;11/11).
Commento: La prescrizione da parte di più medici è associata ad abuso e dipendenza dagli oppioidi prescritti (Cragg et al., 2019).
2.2 Titolazione: I medici che prescrivono oppioidi dovrebbero considerare di iniziare il trattamento con dosi basse (<50 mg di morfina equivalente/d). Dichiarazione di buona pratica clinica. Consenso/forte consenso (15/16;11/11).
Commento: Esistono diversi strumenti pratici per il calcolo dei milligrammi equivalenti di morfina (MME). Essi differiscono nei dosaggi di MME basati su studi a dose singola in individui sani e possono variare considerevolmente. Pertanto, questi strumenti pratici devono essere utilizzati solo come guida. Quando si passa da un oppioide a un altro, i rapporti di conversione devono sempre essere utilizzati con cautela.
Strumento pratico: Calcolo dei milligrammi equivalenti di morfina.
https://www.cdc.gov/drugoverdose/training/dosing/
app: http://www.opioidcalculator.com.au
2.3 Titolazione: I medici che prescrivono gli oppioidi devono considerare di aumentare le dosi in modo graduale per raggiungere l'obiettivo terapeutico individuale, a seconda dell'efficacia e della tollerabilità. Dichiarazione di buona pratica clinica. Forte consenso (16/16;11/11).
Commento: Una modalità graduale potrebbe essere un aumento del 25% entro 3-8 giorni.
2.4 Responsivi al trattamento e dose ottimale: I medici e i pazienti devono considerare che una dose ottimale è quella che raggiunge gli obiettivi terapeutici predefiniti con eventi avversi minimi o tollerabili (=rispondente al trattamento). Dichiarazione di buona pratica clinica. Forte consenso (17/17;12/12).
Commento: La dose ottimale è raggiunta quando un aumento non comporta alcuna riduzione del dolore o miglioramento funzionale.
2.5 Dose massima: Si suggerisce di superare una dose di MME orale >90 mg/d solo in casi eccezionali. Raccomandazione debole. Consenso/consenso forte (14/17; 12/12)
Razionale: Studi osservazionali condotti in Nord America dimostrano un progressivo aumento della probabilità di overdose non fatale non intenzionale o di morte all'aumentare della dose di oppioidi prescritta. Questi esiti gravi sono rari in coloro a cui sono state prescritte dosi inferiori a 50 MEQ/d, ma aumentano in coloro a cui sono state prescritte dosi comprese tra 50 e 90 MEQ/d e, sebbene ancora rari, aumentano ulteriormente in coloro a cui sono state prescritte dosi superiori a 90 MEQ/d (Busse et al., 2017).
Riassunto delle prove:
PICO
Popolazione: Pazienti con dolore cronico non oncologico che iniziano una terapia con oppioidi Intervento: Limitare la dose di oppioidi a una particolare dose massima. Comparatore: Nessuna dose massima di oppioidi.
La meta-regressione dei confronti all'interno dei trial di diverse dosi di oppioidi ha rilevato un'evidenza di qualità moderata contro un effetto dose-risposta per il sollievo dal dolore o il recupero funzionale (Busse et al. 2017).
I dosaggi giornalieri negli studi di estensione a lungo termine in aperto sono stati i seguenti: Buprenorfina transdermica (5-40 µg/h; media 14 µg/h); Idromorfone (8-32 mg/d; media 17 mg/d); Morfina (massimo 90 mg/d, metà dei pazienti ha usato <60 mg/d); Ossicodone: 20-140 mg/d (dosaggi medi negli studi 44 mg/d); Tapentadolo (100-500 mg/d; media 368 mg/d) (Bialas et al., 2020).
È probabile un aumento dose-dipendente del rischio di overdose non fatale da oppioidi: 0,2% per <20 mg MED/die; 0,7% per 50-99 mg MED/die; e 1,8% per ≥100 mg MED/die. Il rischio di overdose fatale da oppioidi aumenta con dosi più elevate: 0,1% per <20 mg MED/die; 0,14% per 20-49 mg MED/die; 0,18% per 50-99 mg MED/die; e 0,23% per ≥100 mg MED/die (Busse et al., 2017). Negli studi che mostrano un aumento dose-dipendente dei rischi si deve tenere conto del confondimento dovuto all'indicazione (i casi più gravi ricevono dosaggi più elevati di oppioidi) (Ranapurwala et al., 2019). Sulla base di questi dati, le attuali linee guida raccomandano una rivalutazione clinica del seguente dosaggio che sono superati: Francia e Germania: >120 mg MEQ/die (Francia: Consultazione specialistica >150 mg MEQ/d) (Häuser et al., 2020; Moisset & Martinez, 2016) e USA e Canada >90 MEQ/d (Busse et al., 2017; Dowell et al., 2016).
Esiste un'ampia variabilità nella risposta del paziente ai farmaci antidolorifici, che può essere correlata all'origine del dolore, alla sensibilità al dolore, alle differenze culturali, al peso, all'età e all'uso precedente di oppiacei, nonché ai polimorfismi genetici. Gli enzimi che metabolizzano i farmaci sono comunemente influenzati da variazioni genetiche. Gli enzimi CYP450, CYP3A4 (fentanil) e CYP2D6 (codeina, idrocodone, ossicodone, tramadolo) sono coinvolti nel metabolismo degli oppioidi (Agarwal et al., 2017). Alcuni pazienti (ad esempio metabolizzatori rapidi) potrebbero richiedere dosaggi più elevati di oppioidi rispetto a quelli raccomandati dalle linee guida.
Questa raccomandazione non affronta o suggerisce l'interruzione degli oppioidi già prescritti a dosaggi più elevati né giustifica l'interruzione improvvisa delle prescrizioni o della copertura degli oppioidi.
2.6 Rotazione degli oppioidi. In caso di inadeguato sollievo dal dolore o di intollerabile tossicità/effetti avversi correlati agli oppioidi, deve essere preso in considerazione il passaggio a un oppioide alternativo (rotazione degli oppioidi). Dichiarazione di buona pratica clinica. Consenso/Consenso forte (14/15; 10/10).
Commento: Le prove a sostegno della pratica del cambio di oppioidi sono in gran parte aneddotiche o basate su studi osservazionali e non controllati (Treillet et al., 2018). Per i dettagli sulla rotazione degli oppioidi vedere Figura 1 e materiale supplementare 6.
FIGURA 1 - Rotazione degli oppioidi (modificata da Drewes et al. 2013)
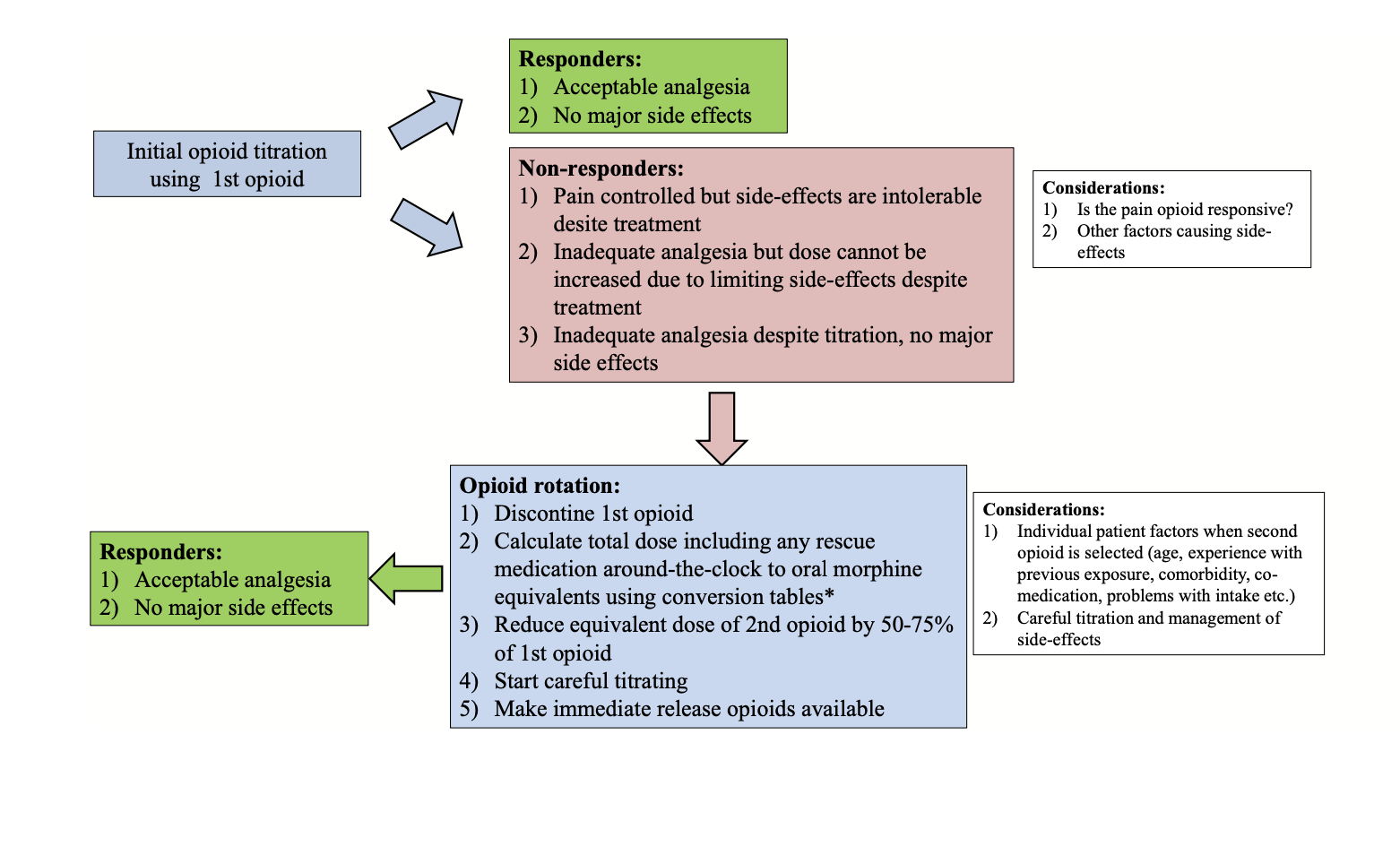
2.7 Indicazione per una potenziale terapia a lungo termine con oppioidi: una terapia della durata di >3 mesi deve essere presa in considerazione solo nei pazienti che rispondono al trattamento (come definito nella Parte 2, Sezione 1.4 sopra). Dichiarazione di buona pratica clinica. Consenso/Forte consenso (16/17; 12/12).
Commento: La decisione di continuare o interrompere la terapia con oppioidi dovrebbe avvenire a 1 mese nella maggior parte dei pazienti. In alcuni pazienti, questa decisione può verificarsi fino a 3 mesi dopo l'inizio dell'assunzione di oppioidi, ad esempio, in caso di un aumento molto lento del dosaggio nel tempo.
- Monitoraggio e documentazione del trattamento
3.1 Monitoraggio regolare del trattamento: durante la LTOT, i medici prescrittori devono considerare di rivedere quanto segue a intervalli regolari (almeno una volta ogni tre mesi): (1) se gli obiettivi terapeutici continuano ad essere raggiunti, (2) se ci sono indicazioni di eventi avversi (ad esempio perdita di libido o cambiamenti psicologici come perdita di interesse, ipomnesi o cadute), o (3) evidenza di disturbo da uso di oppioidi o uso non medico. Dichiarazione di buona pratica clinica. Forte consenso (17/17; 12/12).
3.2 Screening delle droghe nelle urine: lo screening delle droghe nelle urine deve essere preso in considerazione quando si sospetta l'uso non medico di oppioidi prescritti e/o l'uso di droghe illecite. Dichiarazione di buona pratica clinica. Forte consenso (17/17; 12/12).
Commento: Considerare lo screening per le seguenti sostanze: anfetamine, metanfetamine, benzodiazepine, barbiturici, marijuana, cocaina e fenciclidina.
- Interruzione del trattamento con oppioidi
4.1 Interruzione di uno studio sugli oppioidi (<12 settimane): se i singoli obiettivi terapeutici non vengono raggiunti durante la fase di titolazione (massimo 12 settimane) o dopo la rotazione verso un altro oppioide o se si verificano eventi avversi non sufficientemente trattabili o intollerabili (a giudizio del paziente o del medico), il trattamento con analgesici contenenti oppioidi deve essere preso in considerazione per l'interruzione graduale. Dichiarazione di buona pratica clinica. Forte consenso (17/17; 12/12).
4.2 Interruzione del trattamento >12 settimane
Il trattamento a lungo termine deve essere preso in considerazione per l'interruzione graduale se:
- I singoli obiettivi terapeutici non sono più raggiunti, o si verificano eventi avversi non sufficientemente trattabili o intollerabili (secondo il parere del paziente o del medico),
- Gli obiettivi terapeutici individuali sono raggiunti da altri trattamenti medici, fisioterapici, fisici o psicoterapeutici.
- La persona a cui sono stati prescritti oppioidi rifiuta i test delle urine per i farmaci in caso di sospetto uso non medico di oppioidi prescritti.
- La persona a cui sono stati prescritti oppioidi devia o utilizza gli oppioidi in modo non medico nonostante il trattamento complementare da parte di uno specialista della dipendenza.
Dichiarazione di buona pratica clinica. Forte consenso (17/17; 12/12).
4.2 Riduzione dei farmaci
Dopo 6 mesi di trattamento con oppioidi con una buona risposta, può essere presa in considerazione una riduzione della dose con il paziente, per valutare l'indicazione al proseguimento del trattamento e la risposta ai trattamenti non farmacologici (ad es. terapia multimodale) utilizzati in parallelo. Dichiarazione di buona pratica clinica. Forte consenso (17/17; 12/12).
Le principali raccomandazioni per una buona pratica clinica sono riassunte nella tabella 4.
TABELLA 4 - Oppioidi per il dolore cronico non oncologico – un riassunto
1. Valutazione clinica completa
a. Storia medica e psicosociale
b. Visita medica e, se necessario, psicologica e fisioterapica
c. Esami tecnici
d. Valutazione interdisciplinare, se necessario
2. Inizia il trattamento
a. Educazione
b. Terapie non farmacologiche
c, Non oppioidi se necessario
3. Considerare una sperimentazione con oppioidi se
a. Esiste un'indicazione relativa per gli oppioidi per il tipo di sindrome del dolore del paziente e
b. Il trattamento non farmacologico e gli analgesici non oppioidi sono
(i) Non efficace e/o
(ii) Non tollerato e/o
(iii) Controindicato
4. Processo decisionale condiviso con i pazienti
a. Valutare il rapporto rischio/beneficio individuale
b. Considerare le preferenze terapeutiche del paziente
c. Ottenere il consenso e l'accordo informato
d. Stabilire obiettivi di trattamento individuali e realistici (miglioramento del funzionamento quotidiano, riduzione del dolore)
5. Fase iniziale di aggiustamento della dose (8-12 settimane)
a. Iniziare lentamente, andare piano
b. Monitorare e trattare gli effetti collaterali, se necessario
c. Trovare il dosaggio ottimale (obiettivi di trattamento predefiniti raggiunti; assenza di effetti collaterali o effetti tollerabili/gestibili).
d. Interrompere se
(i) non vengono raggiunti gli obiettivi terapeutici predefiniti
(ii) si verificano effetti collaterali intollerabili/gestibili
(iii) si fa un uso non medico degli oppioidi prescritti.
6. Terapia con oppioidi a lungo termine (>12 settimane)
a. Valutazioni regolari (almeno ogni 3 mesi)
b. Valutare le quattro A: Attività, analgesia, comportamento aberrante, effetti avversi
c. Promuovere terapie non farmacologiche
d. Continuare se
(i) dosaggio stabile
(ii) Miglioramento duraturo delle funzioni quotidiane e riduzione del dolore
(iii) effetti collaterali tollerabili/gestibili
(iv) nessun segnale di uso non medico degli oppioidi prescritti
e. Discutere con il paziente il tapering/la sospensione del farmaco dopo 6 mesi f. Interrompere se
(i) Aumento della dose
(ii) Perdita del miglioramento delle funzioni quotidiane e della riduzione del dolore
(iii) effetti collaterali tollerabili/gestibili
(iv) segnali di uso non medico degli oppioidi prescritti
4 | DISCUSSIONE
Discutiamo alcune somiglianze e differenze tra le linee guida esistenti, comprese quelle del Canada, del CDC degli Stati Uniti e delle raccomandazioni di pratica clinica europea.
Ambito e pubblico: tutte le linee guida esistenti mirano a promuovere la prescrizione responsabile di oppioidi per promuovere la sicurezza delle persone con dolore cronico. Tutti i documenti coprono CNCP, anche se il titolo della linea guida CDC è "dolore cronico". Le linee guida canadesi e CDC sono valide per gli adulti con CNCP, mentre le raccomandazioni europee includono anche bambini e adolescenti. Le linee guida canadesi sono state riviste e le linee guida CDC sono state sviluppate per ridurre l'epidemia di oppioidi in Canada e negli Stati Uniti. Le raccomandazioni europee sono state redatte per aiutare a prevenire un'epidemia di oppioidi da prescrizione in Europa. Il pubblico target delle linee guida CDC sono i medici di base, mentre le raccomandazioni canadesi ed europee sono rivolte a tutti gli operatori sanitari coinvolti nella cura delle persone con CNCP.
Composizione del pannello delle linee guida: La linea guida canadese era uno studio avviato dallo sperimentatore. I documenti statunitensi ed europei sono stati sviluppati da un'organizzazione ombrello (CDC e EFIC, rispettivamente). Tutte le linee guida / documenti di posizione sono stati prodotti da un gruppo di esperti medici di diverse specialità. Il fondo fiduciario europeo comprendeva altri professionisti della salute (ad esempio infermieristica, psicologia clinica). Il Canada e l'Europa hanno incluso un rappresentante dei pazienti nel comitato direttivo e diverse misure di coinvolgimento dei pazienti. Il Canada e l'Europa includevano esperti che consideravano gli oppioidi come aventi un ruolo importante e molti che vedevano la pratica con scetticismo.
Coinvolgimento di altre organizzazioni e revisioni: il gruppo delle linee guida canadesi ha incluso il contributo di due associazioni mediche canadesi per le dichiarazioni di pratica clinica. Il CDC ha invitato i partner federali e le parti interessate a commentare. Le raccomandazioni europee sono state approvate da organizzazioni scientifiche di diversi operatori sanitari. Tutte le linee guida / raccomandazioni erano aperte ai commenti pubblici. Le raccomandazioni europee hanno invitato esperti medici europei e nordamericani a rivedere.
Gestione dei conflitti di interesse: tutti i documenti richiedevano una dichiarazione di conflitto di interessi di tutti i membri del gruppo di esperti. CDC ha escluso gli esperti che avevano un rapporto finanziario o promozionale con una società che ha realizzato un prodotto che potrebbe essere interessato dalla linea guida. L'impatto potenziale dei COI finanziari nelle raccomandazioni europee può essere concluso dalla forza del consenso valutata separatamente per l'intero gruppo di linee guida e quelli senza COI finanziari. Il CDC ha esaminato attentamente potenziali conflitti non finanziari (ad esempio proprietà intellettuale, viaggi, dichiarazioni pubbliche o posizioni come la testimonianza del Congresso) per determinare se le attività avrebbero avuto un effetto diretto e prevedibile sulla raccomandazione.
Metodi: Tutte le linee guida/raccomandazioni hanno condotto ricerche sistematiche nella letteratura, eseguito meta-analisi di studi randomizzati controllati con placebo con oppioidi e valutato la qualità delle prove. Le linee guida europee hanno valutato la forza del consenso sulle raccomandazioni e le dichiarazioni di pratica clinica della TF. Il forte consenso di EFIC per GCP e la mancanza di un forte consenso sulla maggior parte delle potenziali indicazioni e controindicazioni riflettono il diverso background clinico e l'esperienza con gli oppioidi per CNCP dei membri della TF. Tutte le linee guida/raccomandazioni hanno utilizzato GRADE per valutare la qualità delle prove per le raccomandazioni basate sull'evidenza. La maggior parte delle linee guida europee per i medici si basavano su una ricerca selettiva della letteratura e sul consenso degli esperti.
Contenuto complessivo: il Canada ha prodotto 10, CDC 12 e l'Europa sei raccomandazioni basate su prove. Il Canada ha offerto 10 linee guida di esperti basate sull'evidenza e 60 dichiarazioni di buona pratica clinica in Europa.
Ruolo degli oppioidi nella gestione della CNCP: tutte le linee guida / raccomandazioni raccomandano di iniziare una sperimentazione con oppioidi solo se i farmaci non farmacologici e non oppioidi hanno fallito. Le raccomandazioni europee specificavano che i trattamenti stabiliti (raccomandati dalle linee guida) avrebbero dovuto fallire. La convinzione che gli oppioidi siano il farmaco più potente contro il CNCP non è stata supportata da nessuna delle tre linee guida, che hanno dimostrato che gli oppioidi e gli analgesici non oppioidi sono ugualmente efficaci nel ridurre il dolore (con piccole dimensioni dell'effetto). Pertanto, la "scala" analgesica dell'Organizzazione Mondiale della Sanità per il trattamento del dolore antitumorale, che ha posizionato i farmaci antinfiammatori non steroidei (FANS) sul gradino inferiore per il dolore lieve e gli oppioidi sui gradini più alti per il dolore persistente da moderato a grave, non è supportata nel CNCP.
In contrasto con le linee guida nordamericane, le raccomandazioni europee hanno fornito raccomandazioni diverse per diversi tipi di CNCP, ad esempio, per non trattare le sindromi da dolore cronico primario con oppioidi. La prescrizione di alte dosi di oppioidi a pazienti con sindromi dolorose primarie potrebbe essere stato un fattore che ha guidato la crisi degli oppioidi in Nord America. L'inclusione di pazienti con traumi fisici e psicologici, svantaggio sociale e disperazione che possono migliorare le segnalazioni di intensità del dolore può anche aver portato alla prescrizione di più oppioidi (Dasgupta et al., 2018; deWeerdt, 2019; Petzke et al., 2020).
Tutti e tre i documenti hanno definito le regole di interruzione per la terapia con oppioidi.
5 | CONCLUSIONI
Gli oppioidi non sono una panacea per tutti i tipi di CNCP e devono essere utilizzati solo in pazienti con dolore selezionati e supervisionati come parte di un approccio completo, multimodale e multidisciplinare al trattamento. Solo in questo contesto, la terapia con oppioidi può essere uno strumento utile per raggiungere e mantenere un livello ottimale di controllo del dolore in pazienti selezionati. Ostacoli all'accesso fuori posto (per esempio, i pagatori che limitano il rimborso o richiedono autorizzazioni precedenti che comportano lunghi ritardi) possono portare a sofferenze inutili, proprio come la prescrizione eccessivamente zelante di oppioidi può portare a sofferenze inutili.
Come recentemente affermato da Barnett (2020), "il dibattito sulla prescrizione di oppioidi sembra irrimediabilmente polarizzato: o gli oppioidi sono armi di dipendenza di massa sponsorizzate industrialmente o sono un'ultima speranza fraintesa per alleviare la sofferenza. L'uso ottimale dei farmaci si trova tra questi due poli".
Gli oppioidi sono un'arma a doppio taglio. Usati in modo inappropriato (indicazione errata, monitoraggio inappropriato degli effetti positivi e negativi, gestione inadeguata degli effetti collaterali) possono essere associati a danni rilevanti per il paziente. Pertanto, la European Pain Federation chiede una formazione medica continua sull'uso corretto degli oppioidi negli approcci terapeutici multi-professionali e multi-modali. Chiediamo inoltre di migliorare l'accesso e il finanziamento di servizi e terapie completi per il trattamento del dolore e di aumentare i fondi per una solida ricerca nel trattamento del dolore.
RINGRAZIAMENTI
Gli autori ringraziano Sarah Badreh, Melinda Borzsak-Schramm, Christel Geevels e Sam Kynman (ufficio esecutivo dell'EFIC) per il supporto organizzativo.
CONFLITTI DI INTERESSE
Eric Buchser ha ricevuto finanziamenti per la ricerca da Medtronic. Geert Dom ha ricevuto onorari personali per le attività del comitato consultivo da Janssen (Belgio). Asborn Drewes: ha ricevuto una borsa di ricerca da Grünenthal, onorari personali per il comitato consultivo e/o attività di relatore da Kyowa-Kirin. Bart Morlion ha ricevuto borse di studio e/o onorari per la ricerca clinica da Novartis, Pfizer, Janssen, Shionogi; per le attività di relatore di Grünenthal, Lilly, Mundipharma, Pfizer e per le attività di consulenza di Astellas, Boehringer Ingelheim, Grünenthal, Janssen, Mundipharma, TEVA, GSK, Kyowa‐Kirin, Pfizer, Liilly, Boston Scientific, P&G. Tony O'Brien ha ricevuto una borsa di studio al Marymount University Hospital & Hospice a sostegno di una conferenza internazionale per celebrare il 150° anniversario della fondazione da parte della Napp Educational Foundation e ha ricevuto onorari personali (conferenze) da Mundipharma, Kyowa Kirin e Shionogi Esther Pogatzi‐ Zahn hanno ricevuto borse di ricerca da Grünenthal e Mundipharma e onorari personali per il comitato consultivo e/o le attività dei relatori da MSD, ArcelRx, Janssen-Cilag e Fresenius Kabi. Thomas Tölle TT ha ricevuto onorari per consulenze, borse di viaggio e spese di conversazione per AOP Orphan, Almiral Hermal, Bionest Partners, Benkitt Renkiser, Grünenthal, Hexal, Indivior, Kaia Health, Lilly, Medscape, Mundipharma, MSD, Novartis, Pfizer, Recordati Pharma, Sanofi-Aventis e TAD Pharma. Gli altri autori non hanno conflitti di interesse finanziari da dichiarare.
CONTRIBUTI DEGLI AUTORI
WH ha eseguito la ricerca di letteratura. Tutti gli autori hanno partecipato allo sviluppo delle raccomandazioni di pratica clinica. NKS, KV e WH hanno scritto il manoscritto. Tutti gli autori hanno discusso e commentato il manoscritto.
Traduzione in italiano a cura di Caterina Aurilio e Lorenza Saini
BIBLIOGRAFIA
- Agarwal, D. , Udoji, M. A. , & Trescot, A. (2017).Genetic testing for opioid pain management: A primer. Pain and Therapy, 6, 93–105. 10.1007/s40122-017-0069-2 [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Andrews, J. C. , Schünemann, H. J. , Oxman, A. D. , Pottie, K. , Meerpohl, J. J. , Coello, P. A. , Rind, D. , Montori, V. M. , Brito, J. P. , Norris, S. , Elbarbary, M. , Post, P. , Nasser, M. , Shukla, V. , Jaeschke, R. , Brozek, J. , Djulbegovic, B. , & Guyatt, G. (2013).GRADE guidelines: 15. Going from evidence to recommendation‐determinants of a recommendation's direction and strength. Journal of Clinical Epidemiology, 66, 726–735. 10.1016/j.jclinepi.2013.02.003 [PubMed] [CrossRef] [Google Scholar]
- Ashina, S. (2019). Opioid use among people with migraine: Results of the OVERCOME study. Presented at: American Headache Society Annual Scientific Meeting; July 11–14, Philadelphia.
- Ballantyne, J. C. , & Sullivan, M. D. (2015). Intensity of chronic pain – The wrong metric?New England Journal of Medicine, 373, 2098– 10.1056/NEJMp1507136 [PubMed] [CrossRef] [Google Scholar]
- Ballantyne, J. C. (2016). Avoiding opioid analgesics for treatment of chronic low back pain.JAMA, 315, 2459–2460. 10.1001/jama.2016.6753 [PubMed] [CrossRef] [Google Scholar]
- Bally, M. , Dendukuri, N. , Rich, B. , Nadeau, L. , Helin‐Salmivaara, A. , Garbe, E. , & Brophy, J. M. (2017). Risk of acute myocardial infarction with NSAIDs in real world use: Bayesian meta‐analysis of individual patient data.BMJ, 357, j1909. 10.1136/bmj.j1909 [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Barnett, M. L. (2020). Opioid prescribing in the midst of crisis – Myths and realities.New England Journal of Medicine, 382, 1086– 10.1056/NEJMp1914257 [PubMed] [CrossRef] [Google Scholar]
- Bedene, A. , Lijfering, W. M. , Niesters, M. , van Velzen, M. , Rosendaal, F. R. , Bouvy, M. L. , Dahan, A. , & van Dorp, E. L. A. (2019).Opioid prescription patterns and risk factors associated with opioid use in the Netherlands. JAMA Network Open, 2019(2), e1910223. 10.1001/jamanetworkopen.2019.10223 [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Bennett, M. I. , Eisenberg, E. , Ahmedzai, S. H. , Bhaskar, A. , O'Brien, T. , Mercadante, S. , Krčevski Škvarč, N. , Vissers, K. , Wirz, S. , Wells, C. , & Morlion, B. (2019).Standards for the management of cancer‐related pain across Europe‐A position paper from the EFIC Task Force on Cancer Pain. European Journal of Pain, 23, 660–668. 10.1002/ejp.1346 [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Bennett, R. M. , Kamin, M. , Karim, R. , & Rosenthal, N. (2003). Tramadol and acetaminophen combination tablets in the treatment of fibromyalgia pain: A double‐blind, randomized, placebo‐controlled study.American Journal of Medicine, 114, 537–545. 10.1016/S0002-9343(03)00116-5 [PubMed] [CrossRef] [Google Scholar]
- Bialas, P. , Maier, C. , Klose, P. , & Häuser, W. (2020). Efficacy and harms of long‐term opioid therapy in chronic non‐cancer pain: Systematic review and meta‐analysis of open‐label extension trials with a study duration ≥26 weeks.European Journal of Pain, 24, 265–278. 10.1002/ejp.1496 [PubMed] [CrossRef] [Google Scholar]
- Bilal, M. , Chatila, A. , Siddiqui, M. T. , Al‐Hanayneh, M. , Shah, A. R. , Desai, M. , Wadhwa, V. , Parupudi, S. , Casey, B. W. , Krishnan, K. , & Hernandez‐Barco, Y. G. (2019).Rising prevalence of opioid use disorder and predictors for opioid use disorder among hospitalized patients with chronic pancreatitis. Pancreas, 48, 1386–1392. 10.1097/MPA.0000000000001430 [PubMed] [CrossRef] [Google Scholar]
- Bruera, E. , Macmillan, K. , Hanson, J. , & MacDonald, R. N. (1989).The cognitive effects of the administration of narcotic analgesics in patients with cancer pain. Pain, 39, 13–16. 10.1016/0304-3959(89)90169-3 [PubMed] [CrossRef] [Google Scholar]
- Burr, N. E. , Smith, C. , West, R. , Hull, M. A. , & Subramanian, V. (2018).Increasing prescription of opiates and mortality in patients with inflammatory bowel diseases in England. Clinical Gastroenterology and Hepatology, 16, 534–1. [PubMed] [Google Scholar]
- Busse, J. W. , Craigie, S. , Juurlink, D. N. , Buckley, D. N. , Wang, L. , Couban, R. J. , Agoritsas, T. , Akl, E. A. , Carrasco‐Labra, A. , Cooper, L. , Cull, C. , da Costa, B. R. , Frank, J. W. , Grant, G. , Iorio, A. , Persaud, N. , Stern, S. , Tugwell, P. , Vandvik, P. O. , … Calingaert, B. (2012).Individual NSAIDs and upper gastrointestinal complications: A systematic review and meta‐analysis of observational studies (the SOS project). Drug Safety, 35, 1127–1146. 10.1007/BF03261999 [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Busse, J. W. , Craigie, S. , Juurlink, D. N. , Buckley, D. N. , Wang, L. , Couban, R. J. , Agoritsas, T. , Akl, E. A. , Carrasco‐Labra, A. , Cooper, L. , Cull, C. , da Costa, B. R. , Frank, J. W. , Grant, G. , Iorio, A. , Persaud, N. , Stern, S. , Tugwell, P. , Vandvik, P. O. , & Guyatt, G. H. (2017).Guideline for opioid therapy and chronic noncancer pain. Canadian Medical Association Journal, 189, E659–E666. [PMC free article] [PubMed] [Google Scholar]
- Castellsague, J. , Riera‐Guardia, N. , Calingaert, B. , Varas‐Lorenzo, C. , Fourrier‐Reglat, A. , Nicotra, F. , Sturkenboom, M. , & Perez‐Gutthann, S. (2012). Safety of Non‐Steroidal Anti‐Inflammatory Drugs (SOS) Project. Individual NSAIDs and upper gastrointestinal complications: a systematic review and meta‐analysis of observational studies (the SOS project).Drug Safety, 35, 1127–46. [PMC free article] [PubMed] [Google Scholar]
- Chenaf, C. , Kaboré, J. L. , Delorme, J. , Pereira, B. , Mulliez, A. , Zenut, M. , Delage, N. , Ardid, D. , Eschalier, A. , & Authier, N. (2019).Prescription opioid analgesic use in France: Trends and impact on morbidity‐ European Journal of Pain, 23, 124–134. 10.1002/ejp.1291 [PubMed] [CrossRef] [Google Scholar]
- Chou, R. , Deyo, R. , Friedly, J. , Skelly, A. , Weimer, M. , Fu, R. , Dana, T. , Kraegel, P. , Griffin, J. , & Grusing, S. (2017).Systemic pharmacologic therapies for low back pain: A systematic review for an American College of Physicians Clinical Practice Guideline. Annals of Internal Medicine, 166, 480–492. 10.7326/M16-2458 [PubMed] [CrossRef] [Google Scholar]
- Chou, R. , Hartung, D. , Turner, J. , Blazina, I. , Chan, B. , Levander, X. , McDonagh, M. , Selph, S. , Fu, R. , & Pappas, M. (2020).Opioid treatments for chronic pain. Agency for Healthcare Research and Quality (US). [Google Scholar]
- Coates, M. D. , Seth, N. , Clarke, K. , Abdul‐Baki, H. , Mahoney, N. , Walter, V. , Regueiro, M. D. , Ramos‐Rivers, C. , Koutroubakis, I. E. , Bielefeldt, K. , & Binion, D. G. (2020).Opioid analgesics do not improve abdominal pain or quality of life in Crohn's disease. Digestive Diseases and Sciences, 65(8), 2379–2387. 10.1007/s10620-019-05968-x [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Cragg, A. , Hau, J. P. , Woo, S. A. , Kitchen, S. A. , Liu, C. , Doyle‐Waters, M. M. , & Hohl, C. M. (2019).Risk factors for misuse of prescribed opioids: A systematic review and meta‐ Annals of Emergency Medicine, 74, 634–646. 10.1016/j.annemergmed.2019.04.019 [PubMed] [CrossRef] [Google Scholar]
- Darr, U. , & Sussman, N. L. (2020). Drug‐induced liver injury in the setting of analgesic use.Clinics in Liver Disease, 2020(24), 121–129. 10.1016/j.cld.2019.09.008 [PubMed] [CrossRef] [Google Scholar]
- Dasgupta, N. , Beletsky, L. , & Ciccarone, D. (2018).Opioid crisis: No easy fix to its social and economic determinants. American Journal of Public Health, 108, 182–186. 10.2105/AJPH.2017.304187 [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- DeWeerdt, S. (2019).Tracing the US opioid crisis to its roots. Nature, 573, S10– 10.1038/d41586-019-02686-2 [PubMed] [CrossRef] [Google Scholar]
- Dowell, D. , Haegerich, T. M. , & Chou, R. (2016).CDC guideline for prescribing opioids for chronic pain–United States, 2016. JAMA, 315, 1624–1645. 10.1001/jama.2016.1464 [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Drewes, A. M. , Jensen, R. D. , Nielsen, L. M. , Droney, J. , Christrup, L. L. , Arendt‐Nielsen, L. , Riley, J. , & Dahan, A. (2013). Differences between opioids: Pharmacological, experimental, clinical and economical perspectives.British Journal of Clinical Pharmacology, 75, 60–78. [PMC free article] [PubMed] [Google Scholar]
- Drewes, A. M. , Bouwense, S. A. W. , Campbell, C. M. , Ceyhan, G. O. , Delhaye, M. , Demir, I. E. , Garg, P. K. , van Goor, H. , Halloran, C. , Isaji, S. , Neoptolemos, J. P. , Olesen, S. S. , Palermo, T. , Pasricha, P. J. , Sheel, A. , Shimosegawa, T. , Szigethy, E. , Whitcomb, D. C. , & Yadav, D. (2017).Guidelines for the understanding and management of pain in chronic pancreatitis. Pancreatology, 17, 720–731. 10.1016/j.pan.2017.07.006 [PubMed] [CrossRef] [Google Scholar]
- Farmer, A. D. , Drewes, A. M. , Chiarioni, G. , De Giorgio, R. , O'Brien, T. , Morlion, B. , & Tack, J. (2019).Pathophysiology and management of opioid‐induced constipation: European expert consensus statement. United European Gastroenterology Journal, 7, 7–20. 10.1177/2050640618818305 [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Finnerup, N. B. , Attal, N. , Haroutounian, S. , McNicol, E. , Baron, R. , Dworkin, R. H. , Gilron, I. , Haanpää, M. , Hansson, P. , Jensen, T. S. , Kamerman, P. R. , Lund, K. , Moore, A. , Raja, S. N. , Rice, A. S. C. , Rowbotham, M. , Sena, E. , Siddall, P. , Smith, B. H. , & Wallace, M. (2015).Pharmacotherapy for neuropathic pain in adults: A systematic review and meta‐ The Lancet Neurology, 14, 162–173. 10.1016/S1474-4422(14)70251-0 [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Fitzcharles, M. A. , Faregh, N. , Ste‐Marie, P. A. , & Shir, Y. (2013).Opioid use in fibromyalgia is associated with negative health related measures in a prospective cohort study. Pain Res Treat, 2013, 898493. 10.1155/2013/898493 [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Fitzcharles, M. A. , Perrot, S. , & Häuser, W. (2018). Comorbid fibromyalgia: A qualitative review of prevalence and importance.European Journal of Pain, 22, 1565–1576. 10.1002/ejp.1252 [PubMed] [CrossRef] [Google Scholar]
- Furlan, A. D. , Reardon, R. , & Weppler, C. ; National Opioid Use Guideline Group . (2010).Opioids for chronic noncancer pain: A new Canadian practice guideline. Canadian Medical Association Journal, 182, 923–930. 10.1503/cmaj.100187 [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Gay, C. , Chabaud, A. , Guilley, E. , & Coudeyre, E. (2016). Educating patients about the benefits of physical activity and exercise for their hip and knee osteoarthritis. Systematic literature review.Annals of Physical and Rehabilitation Medicine, 59, 174–183. 10.1016/j.rehab.2016.02.005 [PubMed] [CrossRef] [Google Scholar]
- Goshua, A. , Craigie, S. , Guyatt, G. H. , Agarwal, A. , Li, R. , Bhullar, J. S. , Scott, N. , Chahal, J. , Pavalagantharajah, S. , Chang, Y. , Couban, R. , & Busse, J. W. (2018).Patient values and preferences regarding opioids for chronic noncancer pain: A systematic review. Pain Medicine, 19, 2469– 10.1093/pm/pnx274 [PubMed] [CrossRef] [Google Scholar]
- Häuser, W. , Buchser, E. , Finn, D. , Dom, G. , Fors, E. , Heiskanen, T. , Jarlbaek, L. , Knaggs, R. D. , Kosek, E. , Krcevski‐Škvarč, N. J. , Pakkonen, K. , Perrot, S. D. , Trouvain, A. P. , & Morlion, M. (2021).Is Europe also facing an opioid crisis – A narrative review and survey of European Pain Federation chapters. European Journal of Pain (submitted). [PubMed] [Google Scholar]
- Häuser, W. , Bock, F. , Hüppe, M. , Nothacker, M. , Norda, H. , Radbruch, L. , Schiltenwolf, M. , Schuler, M. , Tölle, T. , Viniol, A. , & Petzke, F. ; Koautoren für die Konsensusgruppe der 2. Aktualisierung der S3‐Leitlinie LONTS . (2020).Recommendations of the second update of the LONTS guidelines: Long‐term opioid therapy for chronic noncancer pain. Schmerz, 34, 204–244. [PubMed] [Google Scholar]
- Kaiser, U. , Treede, R. D. , & Sabatowski, R. (2017).Multimodal pain therapy in chronic noncancer pain‐gold standard or need for further clarification? Pain, 158, 1853– 10.1097/j.pain.0000000000000902 [PubMed] [CrossRef] [Google Scholar]
- Kalkman, G. A. , Kramers, C. , van Dongen, R. T. , van den Brink, W. , & Schellekens, A. (2019).Trends in use and misuse of opioids in the Netherlands: A retrospective, multi‐source database study. Lancet Public Health, 4, e498– [PubMed] [Google Scholar]
- Karmali, R. N. , Bush, C. , Raman, S. R. , Campbell, C. I. , Skinner, A. C. , & Roberts, A. W. (2020).Long‐term opioid therapy definitions and predictors: A systematic review. Pharmacoepidemiology and Drug Safety, 29, 252– 10.1002/pds.4929 [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Kosek, E. , Cohen, M. , Baron, R. , Gebhart, G. F. , Mico, J. A. , Rice, A. S. , Rief, W. , & Sluka, A. K. (2016).Do we need a third mechanistic descriptor for chronic pain states? Pain, 157, 1382– 10.1097/j.pain.0000000000000507 [PubMed] [CrossRef] [Google Scholar]
- Krcevski‐Škvarc, N. , Morlion, B. , Vowles, K. E. , Bannister, K. , Buchsner, E. , Casale, R. , Chenot, F.‐ , Chumbley, G. , Drewes, A. M. , Dom, G. , Jutila, L. , O'Brien, T. , Pogatzky‐Zahn, E. , Ragusa, M. , Suarez‐Serrano, C. , Tölle, T. , & Häuser, W. (2021). European* clinical practice recommendations on opioids for chronic noncancer pain – Part 2. European Journal of Pain, in press. [PubMed][Google Scholar]
- Langendam, M. W. , Akl, E. A. , Dahm, P. , Glasziou, P. , Guyatt, G. , & Schünemann, H. J. (2013). Assessing and presenting summaries of evidence in Cochrane Reviews.Systematic Reviews, 2, 81. 1186/2046-4053-2-81 [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Lamb, C. A. , Kennedy, N. A. , Raine, T. , Hendy, P. A. , Smith, P. J. , Limdi, J. K. , Hayee, B. H. , Lomer, M. C. E. , Parkes, G. C. , Selinger, C. , Barrett, K. J. , Davies, R. J. , Bennett, C. , Gittens, S. , Dunlop, M. G. , Faiz, O. , Fraser, A. , Garrick, V. , Johnston, P. D. , … Hawthorne, A. B. (2019).British Society of Gastroenterology consensus guidelines on the management of inflammatory bowel disease in adults. Gut, 68(Suppl 3), s1– 10.1136/gutjnl-2019-318484 [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Macfarlane, G. J. , Kronisch, C. , Dean, L. E. , Atzeni, F. , Häuser, W. , Fluß, E. , Choy, E. , Kosek, E. , Amris, K. , Branco, J. , Dincer, F. , Leino‐Arjas, P. , Longley, K. , McCarthy, G. M. , Makri, S. , Perrot, S. , Sarzi‐Puttini, P. , Taylor, A. , & Jones, G. T. (2017).EULAR revised recommendations for the management of fibromyalgia. Annals of the Rheumatic Diseases, 76, 318–328. 1136/annrheumdis-2016-209724 [PubMed] [CrossRef] [Google Scholar]
- Maher, C. , Underwood, M. , & Buchbinder, R. (2017).Non‐specific low back pain. Lancet, 389, 736–747. 10.1016/S0140-6736(16)30970-9 [PubMed] [CrossRef] [Google Scholar]
- Minen, M. T. , Tanev, K. , & Friedman, B. W. (2014).Evaluation and treatment of migraine in the emergency department: A review. Headache: the Journal of Head and Face Pain, 54, 1131– 10.1111/head.12399 [PubMed] [CrossRef] [Google Scholar]
- Moisset, X. , & Martinez, V. (2016).Opioid use for the management of chronic non‐cancer pain: French guidelines. Revue Neurologique, 172, 337–338. 10.1016/j.neurol.2016.05.004 [PubMed] [CrossRef] [Google Scholar]
- Moore, A. R. , Eccleston, C. , Derry, S. , Wiffen, P. , Bell, R. F. , Straube, S. , & McQuay, H. (2010).“Evidence” in chronic pain‐establishing best practice in the reporting of systematic reviews. Pain, 150, 386– 10.1016/j.pain.2010.05.011 [PubMed] [CrossRef] [Google Scholar]
- Moore, R. , Clifford, A. M. , Moloney, N. , Doody, C. , Smart, K. M. , & O'Leary, H. (2020).The relationship between clinical and quantitative measures of pain sensitization in knee osteoarthritis. Clinical Journal of Pain, 36, 336–343. 10.1097/AJP.0000000000000798 [PubMed] [CrossRef] [Google Scholar]
- Niemann, T. , Madsen, L. G. , Larsen, S. , & Thorsgaard, N. (2000).Opioid treatment of painful chronic pancreatitis. International Journal of Pancreatology, 27, 235– [PubMed] [Google Scholar]
- Nicholas, M. , Vlaeyen, J. W. S. , Rief, W. , Barke, A. , Aziz, Q. , Benoliel, R. , Cohen, M. , Evers, S. , Giamberardino, M. A. , Goebel, A. , Korwisi, B. , Perrot, S. , Svensson, P. , Wang, S. J. , & Treede, R. D. (2019).The IASP Taskforce for the Classification of Chronic pain. The IASP classification of chronic pain for ICD‐11: Chronic primary pain. Pain, 160, 28– 10.1097/j.pain.0000000000001390 [PubMed] [CrossRef] [Google Scholar]
- O'Brien, T. , Christrup, L. L. , Drewes, A. M. , Fallon, M. T. , Kress, H. G. , McQuay, H. J. , Mikus, G. , Morlion, B. J. , Perez‐Cajaraville, J. , Pogatzki‐Zahn, E. , Varrassi, G. , & Wells, J. C. (2017).European Pain Federation position paper on appropriate opioid use in chronic pain management. European Journal of Pain, 21, 3–19. [PMC free article] [PubMed] [Google Scholar]
- Olesen, S. S. , Nøjgaard, C. , Poulsen, J. L. , Haas, S. L. , Vujasinovic, M. , Löhr, M. , Lindkvist, B. , Bexander, L. , Gulbinas, A. , Kalaitzakis, E. , Ebrahim, M. , Erchinger, F. , Engjom, T. , Roug, S. , Novovic, S. , Hauge, T. , Waage, A. , Laukkarinen, J. , Parhiala, M. , … Drewes, A. M. ; Scandinavian Baltic Pancreatic Club . (2019).Chronic pancreatitis is characterized by distinct complication clusters that associate with etiological risk factors. American Journal of Gastroenterology, 114, 656–664. 10.14309/ajg.0000000000000147 [PubMed] [CrossRef] [Google Scholar]
- Olesen, S. S. , Nøjgaard, C. , Novovic, S. , Jensen, N. M. , Nørregaard, P. , Dahl, E. E. , Waage, A. , Hauge, T. , Barauskas, G. , Parhiala, M. , Laukkarinen, J. , & Drewes, A. M. (2020). Pain and aetiological risk factors determine quality of life in patients with chronic pancreatitis, but a brick in the puzzle is missing.Pancreatology, 20(7), 30704–30713. 10.1016/j.pan.2020.09.004 [PubMed] [CrossRef] [Google Scholar]
- Oliveira, C. B. , Maher, C. G. , Pinto, R. Z. , Traeger, A. C. , Lin, C.‐ , Chenot, J.‐F. , van Tulder, M. , & Koes, B. W. (2018).Clinical practice guidelines for the management of non‐specific low back pain in primary care: An updated overview. European Spine Journal, 27, 2791–2803. 10.1007/s00586-018-5673-2 [PubMed] [CrossRef] [Google Scholar]
- Petzke, F. , Klose, P. , Welsch, P. , Sommer, C. , & Häuser, W. (2020). Opioids for chronic low back pain: An updated systematic review and meta‐analysis of efficacy, tolerability and safety in randomized placebo‐controlled studies of at least 4 weeks of double‐blind duration. European Journal of Pain,24, 497–517. 10.1002/ejp.1519 [PubMed] [CrossRef] [Google Scholar]
- Ranapurwala, S. I. , Naumann, R. B. , Austin, A. E. , Dasgupta, N. , & Marshall, S. W. (2019).Methodologic limitations of prescription opioid safety research and recommendations for improving the evidence base. Pharmacoepidemiology and Drug Safety, 28, 4– 10.1002/pds.4564 [PubMed] [CrossRef] [Google Scholar]
- Rosner, B. , Neicun, J. , Yang, J. C. , & Roman‐Urrestarazu, A. (2019). Opioid prescription patterns in Germany and the global opioid epidemic: Systematic review of available evidence.PLoS One, 14, e0221153. 10.1371/journal.pone.0221153 [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Russell, I. J. , Kamin, M. , Bennett, R. M. , Schnitzer, T. J. , Green, J. A. , & Katz, W. A. (2000).Efficacy of tramadol in treatment of pain in fibromyalgia. Journal of Clinical Rheumatology, 6, 250–257. 1097/00124743-200010000-00004 [PubMed] [CrossRef] [Google Scholar]
- Schjerning, O. , Rosenzweig, M. , Pottegård, A. , Damkier, P. , & Nielsen, J. (2016).Abuse potential of pregabalin: A systematic review. CNS Drugs, 30, 9–25. 10.1007/s40263-015-0303-6 [PubMed] [CrossRef] [Google Scholar]
- Skelly, A. C. , Chou, R. , & Dettori, J. R. (2018).Noninvasive nonpharmacological treatment for chronic pain: A systematic review. Agency for Healthcare Research and Quality (US). [Google Scholar]
- Sommer, C. , Klose, P. , Welsch, P. , Petzke, F. , & Häuser, W. (2020). Opioids for chronic non‐cancer neuropathic pain. An updated systematic review and meta‐analysis of efficacy, tolerability and safety in randomized placebo‐controlled studies of at least 4 weeks duration.European Journal of Pain, 24, 3–18. 10.1002/ejp.1494 [PubMed] [CrossRef] [Google Scholar]
- Sullivan, M. D. , & Howe, C. Q. (2013).Opioid therapy for chronic pain in the United States: Promises and perils. Pain, 154(Suppl 1), S94–S100. 10.1016/j.pain.2013.09.009 [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Toubia, T. , & Khalife, T. (2019). The endogenous opioid system: Role and dysfunction caused by opioid therapy.Clinical Obstetrics and Gynecology, 62, 3–10. 10.1097/GRF.0000000000000409 [PubMed] [CrossRef] [Google Scholar]
- Treede, R. D. , Rief, W. , Barke, A. , Aziz, Q. , Bennett, M. I. , Benoliel, R. , Cohen, M. , Evers, S. , Finnerup, N. B. , First, M. B. , Giamberardino, M. A. , Kaasa, S. , Korwisi, B. , Kosek, E. , Lavandʼhomme, P. , Nicholas, M. , Perrot, S. , Scholz, J. , Schug, S. , … Wang, S. J. (2019). Chronic pain as a symptom or a disease: The IASP Classification of Chronic Pain for the International Classification of Diseases (ICD‐11). Pain,160, 19– 10.1097/j.pain.0000000000001384 [PubMed] [CrossRef] [Google Scholar]
- Treillet, E. , Laurent, S. , & Hadjiat, Y. (2018).Practical management of opioid rotation and equianalgesia. Journal of Pain Research, 11, 2587–2601. [PMC free article] [PubMed] [Google Scholar]
- Trouvin, A. P. , & Perrot, S. (2019).New concepts of pain. Best Practice & Research Clinical Rheumatology, 33, 01415. [PubMed] [Google Scholar]
- Walitt, B. , Klose, P. , Fitzcharles, M. A. , Phillips, T. , & Häuser, W. (2016). Cannabinoids for fibromyalgia.Cochrane Database Systematic Review, 7, CD011694. 10.1002/14651858.CD011694.pub2 [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Welsch, P. , Sommer, C. , Schiltenwolf, M. , & Häuser, W. (2015). Opioids in chronic noncancer pain‐are opioids superior to nonopioid analgesics? A systematic review and meta‐analysis of efficacy, tolerability and safety in randomized head‐to‐head comparisons of opioids versus nonopioid analgesics of at least four week's duration.Schmerz, 29, 85– [PubMed] [Google Scholar]
- Welsch, P. , Petzke, F. , Klose, P. , & Häuser, W. (2020). Opioids for chronic osteoarthritis pain: An updated systematic review and meta‐analysis of efficacy, tolerability and safety in randomized placebo‐controlled studies of at least 4 weeks double‐blind duration[published correction appears in Eur J Pain, 24; 1420]. European Journal of Pain, 24, 685– [PubMed] [Google Scholar]
- Wiffen, P. J. , Wee, B. , Derry, S. , Bell, R. F. , & Moore, R. A. (2017).Opioids for cancer pain – An overview of Cochrane reviews. Cochrane Database Systematic Review, 7, CD012592. [PMC free article] [PubMed] [Google Scholar]
- Woolf, C. J. (1983).Evidence for a central component of post‐injury pain hypersensitivity. Nature, 306, 686– 10.1038/306686a0 [PubMed] [CrossRef] [Google Scholar]
- Zaccara, G. , Gangemi, P. , Perucca, P. , & Specchio, L. (2011).The adverse event profile of pregabalin: A systematic review and meta‐analysis of randomized controlled trials. Epilepsia, 52, 826–836. 10.1111/j.1528-1167.2010.02966.x [PubMed] [CrossRef] [Google Scholar]
SITOGRAFIA
- American Headache Society (2019).Opioids and migraine. Retrieved from https://americanheadachesociety.org/news/opioids‐migraine/ [Google Scholar]
- Drossman, D. (2019). Understanding and managing pain in irritable bowel syndrome. Retrievedfromhttps://www.aboutibs.org/understanding‐and‐managing‐pain‐in‐ibs.html?showall=1 [Google Scholar]
- European Medicines Agency . (2017).Guideline on the clinical development of medicinal products intended for the treatment of pain. Retrieved from https://www.ema.europa.eu/en/clinical‐development‐medicinal‐products‐intended‐treatment‐pain [Google Scholar]
- National Records of Scotland . (2018).Drug‐related deaths in Scotland. Retrieved from https://www.nrscotland.gov.uk/statistics‐and‐data/statistics/statistics‐by‐theme/vital‐events/deaths/drug‐related‐deaths‐in‐scotland [Google Scholar]
- Ramaekers, J. , Knonche, A. , & Schulze, H. (2006).Effects of medicinal drugs on actual and simulated driving. Retrieved from https://www.bast.de/Druid/EN/deliverales‐list/downloads/Deliverable_1_2_2.pdf?__blob=publicationFile&v=1
- UptoDate . (2020a). Grading tutorial. Retrieved fromhttps://www.uptodate.com/home/grading‐tutorial [Google Scholar]
- UptoDate . (2020b). Management of short bowel syndrome. Retrieved fromhttps://www.uptodate.com/contents/management‐of‐the‐short‐bowel‐syndrome‐in‐adults#H2670286206 [Google Scholar]

